Article | 17/12/2020
L'origine de la vie sur Terre vue par un géologue : quoi de neuf depuis 2015 ?
17/12/2020
Résumé
Traces de vie anciennes, apparition(s) de la vie sur Terre par étapes et environnements possibles, métabolismes hétérotrophes et autotrophes connus et possibles à l'Archéen selon les milieux envisagés.
Table des matières
Avertissement
Cet article sur l'origine de la vie est basé sur une contribution écrite suite à une commande de la revue TDC (Textes et Documents pour la Classe) et plus précisément pour son numéro de novembre 2020 Micro-organismes et biodiversité qui dresse un état des lieux des connaissances et des axes de la recherche les plus récents sur les micro-organismes, et donne quelques pistes concrètes pour enseigner. Les contraintes éditoriales d'une revue “papier” limitaient la taille de cet article à 20 000 signes et 6 figures. Planet-Terre n'ayant pas les mêmes contraintes éditoriales, le papier original a été augmenté/transformé, sans en changer l'esprit, en un article plus étoffé (48 000 signes et 31 figures). Cet article de la revue TDC devait faire le point sur l'état actuel des connaissances, et non pas seulement sur les dernières découvertes ou orientations des années 2015 à 2020. Il y aura donc forcément des redondances avec l'article écrit en 2015 pour l'Encyclopédie de l'Environnement et repris sur Planet-Terre, L'origine de la vie vue par un géologue qui aime l'astronomie. Mais il y aura des données nouvelles, car ce domaine de la géologie avance vite.
Introduction
Jusqu'au XIXe siècle, l'origine de la vie n'était pas une question dans les mondes chrétien, juif et musulman (ordre alphabétique) : tous les organismes vivants, du plus simple au plus complexe, avaient été créés tels quels par un dieu créateur. Les Textes indiquent même dans quel ordre ce Dieu aurait créé les êtres vivants : les plantes le troisième jour, les oiseaux et les poissons le cinquième jour, les animaux terrestres et l'homme le sixième jour. Rien n'est indiqué à propos de la création des bactéries, des archées et des virus ; dommage par les temps qui courent !
Source - © XIIe s. Bible de Souvigny / Médiathèque de Moulins Les premières scènes de la Genèse sont illustrées sur la page de gauche. D'après les Textes, la création de la vie s'est faite en 3 jours : la création des plantes le 3e jour (2e ligne, panneau de gauche), la création des animaux aquatiques et des oiseaux le 5e jour (3e ligne, panneau de gauche), la création des animaux terrestres et de l'homme le 6e jour (3e ligne, panneau de droite). | Source - © XIIe s. Bible de Souvigny / Médiathèque de Moulins À gauche, Dieu crée les créatures marines et les oiseaux (5e jour) ; à droite, Dieu crée les animaux terrestres (6e jour). |
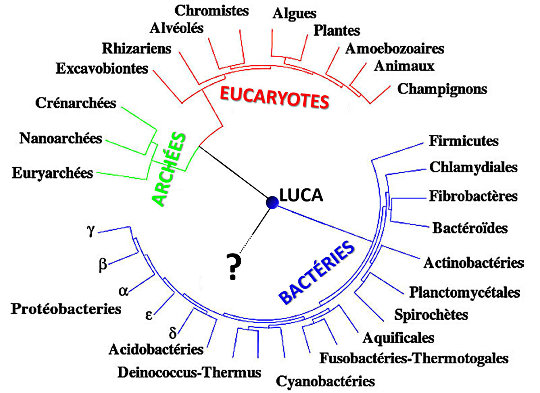
Puis la théorie de l'Évolution fut proposée par Darwin et démontrée par la suite. Tous les êtres qui vivent aujourd'hui descendent, avec force modifications, d'êtres vivants plus anciens. Les études géologiques (les fossiles), biologiques (l'anatomie, la morphologie…), biochimiques (nature, similitudes et différences des gènes et des molécules comme les protéines…) permettent de bâtir un arbre phylogénétique de toutes les espèces actuelles. Cet arbre suggère fortement que toutes les formes de vie d'aujourd'hui descendent d'un très lointain ancêtre théorique unique, baptisé LUCA (Last Universal Common Ancestor). Attention, LUCA n'est pas le plus vieil être vivant terrestre, mais le plus récent des ancêtres communs à tous les êtres vivants actuels ; il y a eu des êtres vivants antérieurs à LUCA.
Source - © 2008 Dosto, modifié
Figure 3. Arbre phylogénétique synthétique de la vie
L'origine de la vie se situe quelque part au niveau du point d'interrogation.
Les plus vieilles traces de vie sur Terre
Les plus vieux fossiles indiscutés d'êtres pluricellulaires datent du Protérozoïque supérieur (environ −0,6 à −0,7 Ga) avec les faunes d'Ediacara, de Doushantuo… On connait des êtres macroscopiques plus vieux comme Grypania (≈ −2,1 Ga), mais on ne sait pas si ce sont des unicellulaires géants ou des êtres pluricellulaires. De probables êtres pluricellulaires quasi contemporains de Grypania ont été trouvés au Gabon en 2010, mais leur nature pluricellulaire probable est encore débattue. Une synthèse sur ces fossiles protérozoïques (faite en 2010) est disponible dans De Burgess à Franceville (Gabon) : les plus anciennes traces fossiles de pluricellulaires.
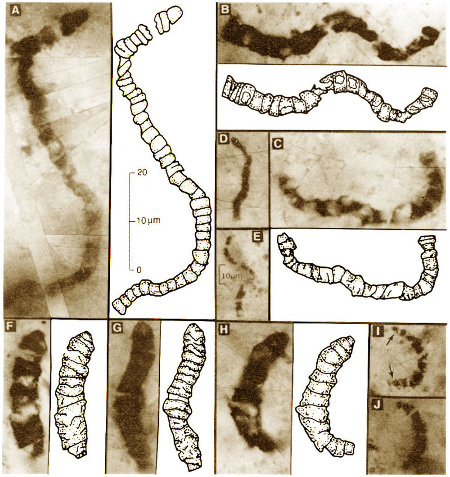
Avant −2,1 Ga, d'après les traces fossiles, c'était le règne exclusif des unicellulaires (surtout des bactéries et des archées, mais sans doute aussi des eucaryotes depuis −2,7 Ga). En Australie, dans le craton de Pilbara (formation de Warrawoona), on connait depuis longtemps des stromatolites âgés de −3,47 Ga. Dans des bancs d'accidents siliceux (des silex) contemporains des stromatolites, on a découvert en 1993 des microfossiles ayant les dimensions et la morphologie des cyanobactéries actuelles. Bien qu'il y ait encore des discussions sur l'âge de ces accidents siliceux (certains pensent qu'ils ne sont pas contemporains des roches sédimentaires encaissantes mais qu'ils ont une origine hydrothermale postérieure), ces microfossiles suggèrent fortement, et les stromatolites contemporains montrent, que la vie cellulaire existait vers −3,5 Ga. Ce sont les plus vieilles traces morphologiques non (ou quasiment pas) discutées de la présence de vie, il y a 3,5 Ga.
Source - © 2005 - ? Macquarie University (Pilbara) - Gilles Dromart | A, B, C, D, E : Primaevifilum amoenum ; F, G, H, I, J : Primaevifilum conicoterminatum. J.W. Schopf, 1993. Microfossils of the Early Archean Apex Chert: New Evidence of the Antiquity of Life, Sciences, 260, 5108, 640-646 [pdf] |
On cherche avec ardeur, et on a découvert, d'autres indices morphologiques plus vieux que −3,5 Ga, mais dont la signification est encore l'objet de débats et de controverses scientifiques.
C'est le cas au Groenland où des structures ressemblant à des stromatolites âgées de 3,7 Ga ont été trouvées en 2016 à Isua. C'est aussi le cas dans la ceinture verte du Nuvvuagittuq (au Québec) où des structures tubulaires ou en rosette interprétables en termes de micro-organismes ont été découvertes en 2017 dans des sédiments hydrothermaux d'âge compris entre −3,75 et −4,28 Ga.
La figure suivante localise ces stromatolites sur l'ensemble de l'affleurement. A.P. Nutman, V.C. Bennett, C.R.L. Friend, M.J. Van Kranendonk, A.R. Chivas , 2016. Rapid emergence of life shown by discovery of 3,700-million-year-old microbial structures, Nature, 537, 535–538 [pdf] | Figure 7. Vue globale d'un rocher avec lamines et petits dômes à Isua (Groenland) Les flèches rouges signalent trois niveaux contenant des petits dômes dont ceux détaillés sur la figure précédente (secteur encadré en rouge). A.P. Nutman, V.C. Bennett, C.R.L. Friend, M.J. Van Kranendonk, A.R. Chivas , 2016. Rapid emergence of life shown by discovery of 3,700-million-year-old microbial structures, Nature, 537, 535–538 [pdf] |
Ces structures ont été trouvées dans la ceinture verte du Nuvvuagittuq au Québec dans d'anciens dépôts de sources hydrothermales d'un âge compris entre 3,77 et 4,28 Ga. Peut-être les plus vieux « fossiles » connus à ce jour. La barre blanche mesure 200 μm. M.S. Dodd, D. Papineau, T. Grenne, J.F. Slack, M. Rittner, F. Pirajno, J. O'Neil, C.T.S. Little, 2017. Evidence for early life in Earth's oldest hydrothermal vent precipitates, Nature, 543, 60–64 [pdf] | |
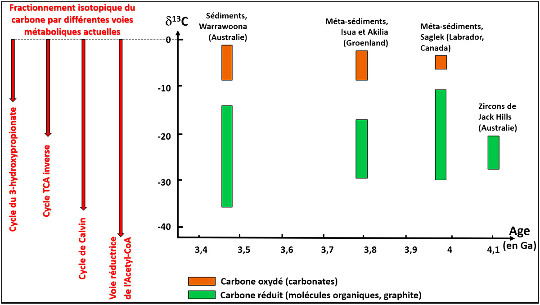
En plus de ces “fossiles” morphologiques, il y a des marqueurs isotopiques. Dans la nature actuelle, la synthèse biologique de molécules organiques à partir de CO2 par les êtres autotrophes fractionne les isotopes du carbone. Les molécules carbonées biogéniques sont légèrement enrichies en carbone léger (12C) par rapport au carbone minéral ambiant. Cet enrichissement se mesure avec l'unité δ (exprimé en ‰), avec δ13C = ([13C/12C]échantillon / [13C/12C]standard] – 1). Ce fractionnement varie de 15 à 40 ‰ suivant les voies métaboliques (cf. Fractionnement isotopique du carbone chez les plantes vasculaires). Il n'est pas modifié (ou très peu) par d'éventuelles modifications de pression et/ou de température ultérieures. Tout au plus est-il un peu réduit par une homogénéisation partielle en cas de métamorphisme à haute température. Dans les sédiments archéens quasiment pas métamorphisés d'Australie et dans des méta-sédiments du Groenland, du Québec…, on trouve des molécules organiques et du graphite (carbone de molécules organiques recristallisé par des évènements métamorphiques ultérieurs) présentant cet enrichissement en carbone “léger” dans des roches de −3,95 Ga, et même dans des zircons australiens de −4,1 Ga. Une vie autotrophe devait exister en ces temps reculés.
Un fractionnement d'une vingtaine de ‰ est bien visible. Pour comparaison, le fractionnement de quatre voies métaboliques actuelles est indiqué à gauche du schéma. Le fractionnement isotopique entre graphite et carbonates dans la ceinture verte du Nuvvuagittuq (−6,7 à −8,3 ‰ pour les carbonates, contre −19,7 à −25,7 ‰ pour le carbone réduit), voisin de celui du Groenland, n'a pas été dessinée à cause de la trop grande incertitude sur l'âge (entre 3,77 et 4,28 Ga).
D'après des données tirées de J.. Schopf, Sciences, 1993, E.A. Bell et al., PNAS 2015 et T. Tashiro et al., Nature 2017.
Les problèmes posés par l'origine de la vie
La Terre étant née à haute température (> 1000°C), elle était forcément stérile à l'origine, il y a 4,5 Ga. Il se pose alors un certain nombre de questions : à partir d'une Terre stérile, où, quand et comment est apparue cette vie ancestrale, les ancêtres de LUCA ?
Ces questions peuvent être abordées d'un point de vue des sciences humaines (études des récits des créations comme le suggèrent les figures 1 et 2…), biochimique… Nous l'aborderons ici avec le regard d'un géologue, qui s'intéresse aussi un peu à l'astronomie et à la biologie.
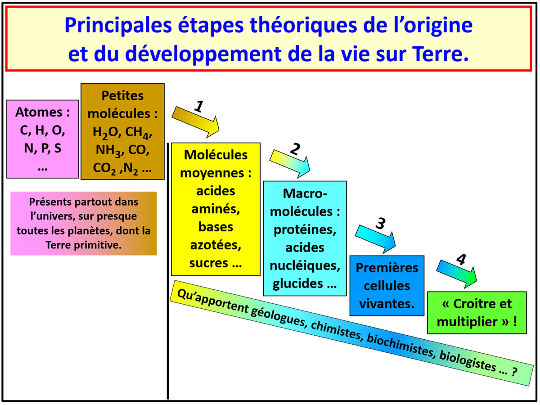
Toutes les formes de vie actuelles sont faites de polymères et autres macromolécules, macromolécules constituées d'enchainements de molécules “moyennes”, comme les acides aminés formant les protéines, les bases azotées, sucres et phosphates formant les acides nucléiques… Ces molécules de taille moyenne, dites prébiotiques, sont constituées de carbone, hydrogène, oxygène, azote, avec un peu de phosphore et de soufre…. Tous ces éléments sont présents et abondants dans l'univers et le système solaire, sous forme de petites molécules (CO, CO2, CH4, H2O, NH3, CNH, N2…). Au départ de la vie, il s'est donc produit, en théorie, une succession de quatre étapes : (1) synthèse ou arrivée de molécules prébiotiques, (2) polymérisation de ces molécules et synthèse de macromolécules, (3) regroupement de ces macromolécules en membranes et agrégats, agrégats dotés de propriétés de réplications et d'échanges de matière et d'énergie, les premières cellules, (4) ces premières cellules ont dû trouver nourriture et/ou énergie pour croitre et se multiplier, pour que la naissance de la vie ne soit pas un « feu de paille » éphémère et que la vie ait pu perdurer.
L'origine des molécules pré-biotiques terrestres
Trois origines sont (ou ont été) envisagées pour les molécules prébiotiques : atmosphérique, extra-terrestre et hydrothermale.
Origine atmosphérique
C'est en 1953 que Miller réalisa ses célèbres expériences. En provoquant des décharges électriques (analogie avec des orages) dans un mélange gazeux censé représenter l'atmosphère primitive de la Terre (supposée comparable à ce qu'on savait à l'époque de l'atmosphère de Jupiter, à savoir H2, CH4, NH3, H2O…), une série de réactions chimiques produisent des molécules organiques, dont des acides aminés. Mais on pense aujourd'hui que l'atmosphère précoce de la Terre contenait très peu d'H2, que la majorité du carbone était sous forme de CO2 et non pas de CH4 …). Et avec un tel mélange, la production de molécules pré-biotiques devient quasi nulle.
Origine extra-terrestre
Des études en radioastronomie montrent que les nébuleuses au sein desquelles naissent les étoiles et les planètes contiennent beaucoup de petites molécules “minérales” (H2O, CO, NH3…) et aussi carbonées (CH4 et autres molécules jusqu'en C3), ainsi que de grosses molécules polycycliques, nommées Polycyclic Aromatic Hydrocarbons (PAHs). Les éventuelles molécules carbonées de taille intermédiaire ne sont pas identifiables avec les techniques actuelles. Dans les parties externes de ces nébuleuses où la température est très basse, les petites molécules forment des glaces (glaces d'eau, de méthane, d'ammoniac…), glaces qui se mélangent avec des poussières de silicates. En théorie comme en laboratoire, si on irradie ces glaces avec des rayons ionisants (ultra-violets, rayons cosmiques…) des réactions à l'état solide ont lieu en leur sein et forment des molécules organiques relativement complexes. La Terre est née du rassemblement de ces poussières (silicatées et glacées) et de petits corps eux-mêmes nés du rassemblement des poussières. Mais la haute température due à l'accrétion a porté la Terre primitive à plus de 1000°C ; les molécules complexes contenues dans ces poussières et petites corps ont dû être détruites. Mais une fois refroidie, la Terre a continué (et continue encore) à recevoir des poussières, des météorites (fragments d'astéroïdes), des comètes (et des poussières cométaires). Ces corps impacteurs, restés de petite taille, sont à priori restés froids et ont conservé leurs molécules organiques. Ce bombardement a été particulièrement intense pendant les 700 premiers millions d'années du système solaire, jusque vers −3,8 Ga, puis s'est fortement ralenti. Les météorites et les comètes d'aujourd'hui sont à priori des “témoins” quasiment intacts de ce qui a percuté la Terre à ces époques reculées, d'où l'intérêt de leur étude dans la recherche des molécules prébiotiques.
Les météorites
On sait depuis longtemps qu'un certain type de météorite, les chondrites carbonées qui représentent environ 5 % des chondrites, sont riches en molécules organiques (jusqu'à 5 % en masse). Cette matière organique est de deux types.
- Des macromolécules organiques insolubles (MOI), insolubles aussi bien dans l'eau que dans des solvants organiques. Ces macromolécules correspondent à 75 à 95 % du total du contenu organique des chondrites carbonées.
- Des molécules organiques “moyennes”, solubles dans l'eau ou dans des solvants organiques. C'est parmi ces molécules moyennes qu'on trouve des molécules prébiotiques. Par exemple, la célèbre météorite de Murchison contient (en masse), environ 60 ppm d'acides aminés répartis en 74 espèces différentes (la vie terrestre n'en utilise qu'une vingtaine), et 1,3 ppm de bases azotées (purines et pyrimidines).
On voit très bien les chondres, aussi bien dans la fracture (à gauche) que sur le plan de coupe (à droite). Cette chondrite, tombée en 1969 dans la municipalité d'Allende (Mexique) est la plus grosse chondrite carbonée jamais tombée sur Terre. Plus de 2 tonnes de fragments (allant de 1 g à 110 kg) ont été récupérés. Elle est relativement pauvre en matière organique (< 1 %). | Source - © 2005 USDoE Figure 12. Fragment de la météorite de Murchison en cours d'étude Des particules issues de la dissolution partielle d'un microfragment décantent au fond du tube. C'est l'analyse de telles solutions qui a révélé les acides aminés et bases azotées. Comme celle d'Allende, cette météorite est aussi tombée sur Terre en 1969, mais en Australie. C'est l'une des météorites les plus riches en molécules organiques prébiotiques. |
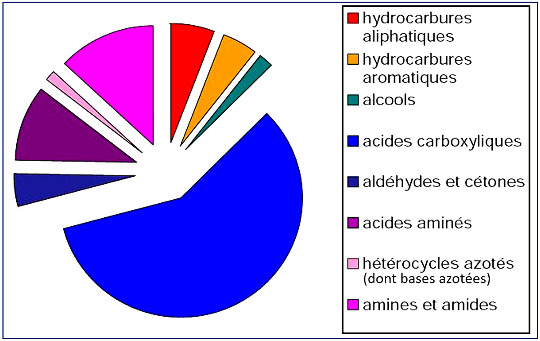
Figure 14. Répartition des composés solubles dans la météorite de Murchison À retrouver dans La matière organique dans les chondrites carbonées. |
Les comètes
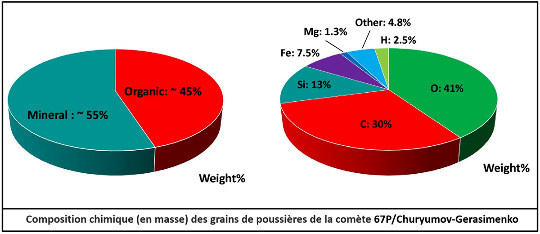
L'analyse des comètes est beaucoup plus récente, car aucun morceau de comète ne tombe intact sur Terre. On a d'abord étudié spectralement la composition de la queue. Puis, en 2006, la mission NASA Stardust a ramené sur Terre quelques milligrammes de poussière cométaire collectée dans la queue de la comète Wild 2. Ces poussières contenaient des silicates et des molécules organiques, dont des cétones, des aldéhydes, des cycles aromatiques, et le plus simple des acides aminés, la glycine. Entre 2014 et 2016, la comète 67P/Churyumov-Gerasimenko (dite Chury) fut étudiée in situ par la sonde européenne Rosetta, malgré l'atterrissage partiellement raté du robot Philae. Des dizaines de molécules organiques volatiles (ne contenant pas plus de trois carbones) ont pu être identifiées dans l'atmosphère de la comète, dont un acide aminé, la glycine. Les poussières ont pu être analysées, mais uniquement vis-à-vis de leur composition élémentaire. Elles sont constituées de composés réfractaires, des silicates et des grosses molécules organiques (de nature inconnue). Les molécules organiques représentent 45 % de la masse de ces poussières ; les atomes de carbone y sont cinq fois plus nombreux que les atomes de silicium. Quatre articles ont été publiés sur Planet-Terre fin 2014 et début 2015, au moment de la mission : La sonde Rosetta explore la comète Churyumov-Gerasimenko. Résultats communiqués au public au bout de 10 semaines d'approche, 1 mois avant l'atterrissage du module Philae, Rosetta et la comète 67P/Churyumov-Gerasimenko : résultats scientifiques publiés à partir des données du survol rapproché d'août et septembre 2014, Comète 67P/Churyumov-Gerasimenko : galerie de paysages et d'objets géologiques photographiés par Rosetta de mi-octobre 2014 à fin janvier 2015, Philae et la comète Churyumov-Gerasimenko (67P/CG) : atterrissage du 12 novembre 2014 et premiers résultats.
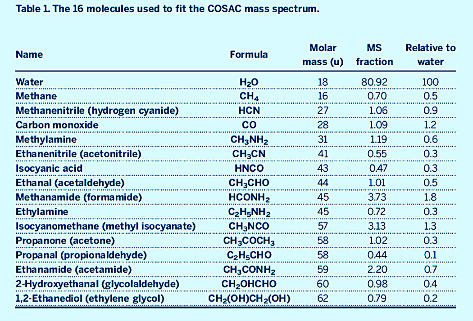
Les gaz (petites molécules volatiles) ont pu être analysés par l'orbiteur Rosetta et par le robot Philae pendant son survol du noyau. Les poussières (composés réfractaires, composés soit de macromolécules organiques, soit de silicates) ont pu être analysées par l'orbiteur Rosetta. Ces 17 images ont été prises le 12 août 2015, à environ 300 km du noyau. | Source - © 2014 ESA/Rosetta/NavCam, modifié – CC BY-SA IGO 3.0 Figure 16. Trajet (approximatif) de l'atterrisseur Philae le 12 novembre 2014 après son atterrissage “raté” L'atterrisseur est arrivé à la surface de la comète avec une vitesse (une lenteur) de 2,5 km/h. Elle aurait dû s'y agripper entre autres avec des grappins, mais cette manœuvre a raté. Philae a rebondi (sans se détériorer) trois fois avant d'aller se coucher derrière un gros bloc. Aucune analyse chimique du sol n'a pu être conduite. Pendant son survol de la comète au-dessus de la face éclairée par le Soleil (donc à une température relativement “élevée” de −40°C), son spectromètre de masse (prévu pour analyser les gaz s'échappant du sol après prélèvement et pyrolyse) a pu analyser les gaz s'échappant de la surface de Chury (cf. figure suivante). |
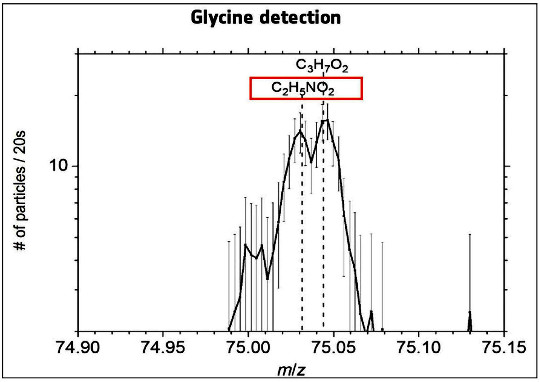
F. Goesmann et al., 2015. Organic compounds on comet 67P/Churyumov-Gerasimenko revealed by COSAC mass spectrometry, Science, 349, 6247, aab0689 | Figure 18. Détection de la glycine par le spectromètre de masse de l'orbiteur Rosetta Après la comète Wild 2, Chury est la deuxième comète où l'on détecte un acide aminé. K. Altwegg et al., 2016. Prebiotic chemicals—amino acid and phosphorus—in the coma of comet 67P/Churyumov-Gerasimenko, Science Advances, 2, 5, e1600285 |
Figure 19. Grains de poussière cométaire issus de Chury et “volant” autour de l'orbiteur Rosetta Cette séquence d'images a été prise le 6 juillet 2015 par la caméra à grand angle OSIRIS. Ce sont ces grains qui ont été captés par la sonde (fig. 20) et analysés (fig. 21). | Figure 20. Grains de poussières sur la surface du collecteur de Rosetta Ces grains ont pu ensuite être analysés un par un par le spectromètre de masse COSIMA (cf. fig. 21). |
Le rapport des masses entre les différents éléments permet de calculer les proportions en nombre de ces atomes, soit 30 % C / 30 % H / 30 % O / 5,5 % Si / 1,6 % Fe / 0,6 % Mg / 2,3 % autres. Le même nombre d'atomes de C et de H suggère l'abondance de noyaux aromatiques (C6H6). Les proportions de Si, O, Fe, Mg suggèrent l'abondance d'olivine et de pyroxène (hydratés). Redessiné d'après : A. Bardyn et al., 2017. Carbon-rich dust in comet 67P/Churyumov-Gerasimenko measured by COSIMA/Rosetta, Monthly Notices of the Royal Astronomical Society, 469, Suppl_2, S712–S722 [pdf] | |
En estimant le flux des comètes, des poussières cométaires, des chondrites carbonées et des poussières interplanétaires pendant les 700 premiers millions d'années, et leur donnant la teneur en matière organique qu'elles ont actuellement, on trouve que la Terre primitive a reçu une masse de matière organique au moins égale à l'ensemble de la biomasse actuelle.
Origine hydrothermale
À haute température (T ≥ 60-70°C) l'eau oxyde le fer réduit (Fe0 rarissime sur Terre, ou Fe2+) en produisant un dégagement de dihydrogène. Suivant l'importance de l'oxydation, on peut obtenir de la magnétite (3 FeO + H2O → Fe3O4 + H2) ou de l'hématite (2 FeO + H2O → Fe2O3 + H2), cf. Le di-hydrogène naturel, une réelle source d'énergie ou un buzz médiatique ?. Le fer contenu dans les silicates est la plupart du temps du Fe2+. Dans les phénomènes hydrothermaux, l'eau réagit avec les silicates, et si ceux-ci contiennent du fer, il se dégage du dihydrogène.
Si on prend la fayalite, le pôle ferreux de l'olivine, on peut écrire la réaction suivante :
- 3 Fe2SiO4 (fayalite) + 2 H2O → 2 Fe3O4 (magnétite) + 3 SiO2 (silice) + 2H2.
Si on prend la forstérite, le pôle magnésien de l'olivine, on peut écrire :
- 2 Mg2SiO4 (forstérite) + 3H2O → Mg3Si2O5(OH)4 (serpentine) + Mg(OH)2 (brucite).
L'olivine usuelle, minéral classique dans la lithosphère océanique et les roches volcaniques continentales, est un mélange forstérite (majoritaire) + fayalite (minoritaire). On peut écrire, de façon qualitative, son altération hydrothermale de la façon suivante :
- olivine + eau → serpentine + magnétite + brucite + dihydrogène.
Or, le dihydrogène réagit avec le dioxyde du carbone pour engendrer des hydrocarbures, principalement du méthane mais aussi des hydrocarbures plus lourds, des aldéhydes… La réaction la plus fréquente, dite de Sabatier, est exothermique et peut s'écrire 4 H2 + CO2 → CH4 + 2 H2O, avec ∆H = −165,0 kJ/mol. Cette réaction est favorisée par des catalyseurs, comme la magnétite, les sulfures… Ce type de réaction peut être réalisée de façon industrielle pour la synthèse d'hydrocarbures (si on dispose de dihydrogène).
Source - © 2018 Ifremer Les gaz de cette source contiennent du CO2 (ce qui est normal en contexte de dorsale), mais aussi 45 % d'H2 et 6 % de CH4. | Dans le sous-sol de ce massif de péridotite (maintenant continentale), des eaux souterraines chargée de HCO3− (issues d'un massif calcaire voisin) réagissent avec les olivines pour donner des serpentines (reconnaissables au premier plan) et ces composés gazeux, cf. Méthane abiotique enflammé et serpentinite du site de la Chimère, Cirali, Turquie). |
D'autres réactions, comme celle dite de Streker, permettent d'obtenir des composés organiques azotés si on ajoute NH3 et CNH à H2 et CO2, et que le milieu a un pH supérieur à 7. Et, expérimentalement, on a réussi à synthétiser des acides aminés dans de tels milieux. Par exemple, si on ajoute à H2 et CO2 de l'azote sous forme d'ammoniac, des oxydes de fer, et s'il y a des gradients de pH non acides et de potentiels redox, L. M. Barge et al. (2019, Redox and pH gradients drive amino acid synthesis in iron oxyhydroxide mineral systems, PNAS, 116, 11, 4828-4833) ont obtenu la synthèse d'alanine, un acide aminé.
Où, dans la nature, trouve-t-on de telles conditions (eau, olivine, CO2, pH neutre ou basique) ? Au niveau de sources hydrothermales à pH neutre ou basique, c'est-à-dire des sources hydrothermales ayant lieu dans des roches très riches en magnésium (péridotites par exemple). En effet, l'altération d'olivine très abondante entraine la production de beaucoup de Mg(OH)2 (brucite), ce qui rend le milieu basique, contrairement à des sources au sein d'un matériel moins riche en magnésium où les sources sont plus acides. De telles sources hydrothermales basiques existent aujourd'hui dans les océans, mais ne sont pas majoritaires. On les trouve en particulier dans les fonds océaniques sans croute (dorsales très lentes), et dans certaines fosses de subduction comme celle des Mariannes (cf. Serpentinisation océanique et vie primitive). On peut aussi en trouver dans certaines régions volcaniques aériennes, et aussi dans le sous-sol de massifs péridotitiques aériens, comme certaines ophiolites (Turquie, Oman…, cf. Méthane abiotique enflammé et serpentinite du site de la Chimère, Cirali, Turquie).
La présence d'acides aminés abiotiques a cessé d'être seulement théorique ou expérimentale en novembre 2018, car des acides aminés ont effectivement été découverts au niveau d'une source hydrothermale. Benedicte Ménez et al. (2018, Abiotic synthesis of amino acids in the recesses of the oceanic lithosphere, Nature 564, 59–63) ont analysé, par des techniques ultrafines de fluorescence UV, des échantillons de serpentines et d'argiles prélevés dans une carotte forée en 2005, forage U1309D, dans le fond océanique de Lost City (champ hydrothermal de la dorsale atlantique sur fond péridotitique). À 175 m sous la surface du fond océanique, des saponites (une variété d'argile) intimement mélangées à des serpentines contiennent des acides aminés aromatiques abiotiques, présents dans des pores internes aux saponites, en particulier du tryptophane. Ces auteurs ont pu démontrer que ces acides aminés n'avaient pas une origine biologique mais provenait de synthèses abiotiques de type réaction de Friedel-Crafts.
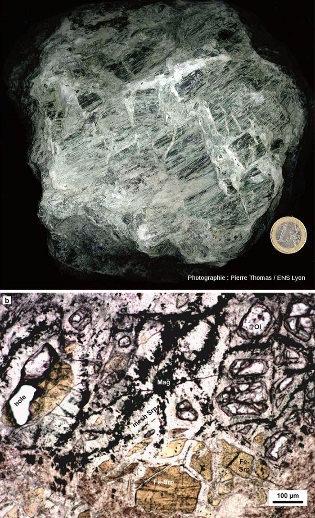
C'est dans de tels contextes qu'a été prélevé en 2005 la carotte étudiée par Bénedicte Menez et al. (2018). Cette étude a permis de montrer qu'il y a actuellement des synthèses abiotiques d'acides aminés aromatiques comme le tryptophane, acides aminés abiotiques qu'il a été très délicat de distinguer des acides aminés “biologiques” abondants dans les secteurs des dorsales. | Ol = olivine, Fe Srp = serpentine riche en fer, mesh srp = trame serpentineuse, Mag = magnétite. P. Thomas, 2013. Le di-hydrogène naturel, une réelle source d'énergie ou un buzz médiatique ?, Planet-Terre, ISSN 2552-9250 Benedicte Ménez et al., 2018. Abiotic synthesis of amino acids in the recesses of the oceanic lithosphere, Nature 564, 59–63 |
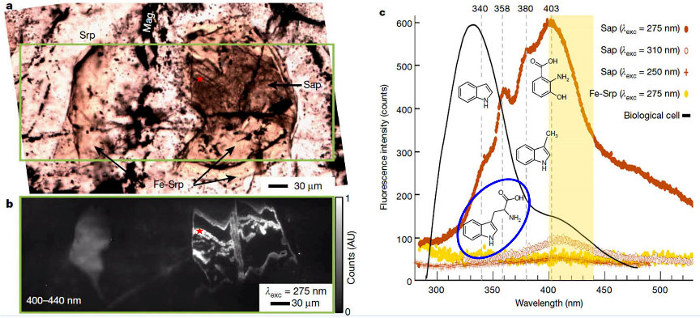
La zone encadrée en vert a été étudié par Synchrotron-coupled Deep-UltraViolet (S-DUV) micro-spectroscopy (micro-spectroscopie en ultra-violet lointain émis par rayonnement synchrotron). (a) Lame mince (LPNA) dans la serpentinite. Srp = serpentine, Fe Srp = serpentine riche en fer, Sap = saponite. (b) Image de la fluorescence (entre 400 et 450 nm) de la surface encadrée en vert sur la figure (a) excitée par des UV de longueur d'onde de 275 nm. L'étoile rouge, au sein de la zone la plus fluorescente, localise la zone quasi ponctuelle dont les spectres de lumière réémises sont figurés sur la figure (c). (c) Trois spectres de fluorescence de la zone ponctuelle figurée par l'étoile rouge des figures (a) et (b), excitée par des longueurs d'onde de 250, 275 et 310 nm. Le spectre de fluorescence (plat) de la serpentine riche en fer a aussi été figuré. La zone jaune correspond aux longueurs d'onde détectées pour obtenir la figure (b). Le spectre de fluorescence excité par des UV de longueur d'onde 275 nm (en brun rouge) montre des pics de fluorescence à 340±6 nm, 358±3 nm, 380±3 nm, et 403±3 nm, correspondant respectivement aux longueurs d'onde de fluorescence de l'indole, du tryptophane, du skatole et de l'acide hydroxy-anthranilique. Les formules de ces quatre composés ont été figurées au niveau de leur longueur d'onde de fluorescence respective. La formule du tryptophane, un acide aminé, a été entourée en bleu. Le spectre de fluorescence des cellules est figuré en noir. Il est principalement dû aux protéines, mélange de polymères d'acides aminés et non pas acides aminés isolés. Benedicte Ménez et al., 2018. Abiotic synthesis of amino acids in the recesses of the oceanic lithosphere, Nature 564, 59–63 | |
Les sources hydrothermales basiques ne sont pas très fréquentes dans la nature actuelle, et ce pour deux raisons principales. D'une part, les sources volcaniques sont riches en composés soufrés, qui s'oxydent en arrivant dans l'eau de mer oxydante ou dans l'atmosphère, donnant ainsi de l'acide sulfurique. D'autre part, les fonds océaniques péridotitiques ne sont pas majoritaires, et les eaux rendues basiques par beaucoup de brucite sont donc minoritaires.
Par contre, à l'Archéen et à l'Hadéen, il n'y avait pas de dioxygène pour oxyder les composés soufrés. Et à l'Archéen et à l'Hadéen, le volcanisme (et donc l'hydrothermalisme associé) était beaucoup plus abondant qu'au Protérozoïque et au Phanérozoïque. De plus, dans ces époques reculées, le volcanisme était fréquemment komatiitiques (cf. Les komatiites, des laves ultrabasiques archéennes, témoins d'une Terre interne très chaude). Or l'altération hydrothermale des komatiites, roches très riches en olivine et en magnésium, devait être très similaire à l'altération des péridotites et l'hydrothermalisme devait générer beaucoup d'eaux basiques.
L'organosynthèse abiotique devait être beaucoup plus abondante il y a 4 Ga que maintenant.
Venues de l'espace ou formées au niveau de sources hydrothermales, les molécules prébiotiques ne devaient pas manquer sur Terre il y a 4 Ga !
Des molécules prébiotiques aux macromolécules puis aux premières cellules
Toutes les cellules actuelles sont constituées de macromolécules (protéines, acides nucléiques…), qui sont des polymères des molécules prébiotiques qui devaient être abondantes sur Terre et dans les océans primitifs d'il y a 4 Ga. Cette polymérisation nécessite une certaine concentration de monomères, et elle est grandement facilitée pour ne pas dire catalysée par certaines surfaces minérales. Expérimentalement, les minéraux les plus efficaces pour catalyser ces diverses polymérisations sont les sulfures (en particulier les sulfures de fer) et les phyllosilicates, surtout les argiles et les serpentines. De plus, les interfeuillets de ces minéraux permettent de concentrer les molécules grâce à des liaisons hydrogènes, et accélèrent ainsi les réactions de condensation-polymérisation. On est là à l'intersection de la minéralogie et de la biochimie. Les sources hydrothermales, profondes ou non, réunissent en un même lieu tout ce qu'il faut pour provoquer cette polymérisation : synthèse des monomères et surfaces minérales de serpentines, d'argiles…
Il y a un deuxième site souvent proposé où a pu avoir lieu cette polymérisation : des mares peu profondes, types mares côtières peu profondes et vaseuses (argileuses). À défaut d'origine hydrothermale, dans ces mares, les molécules prébiotiques pourrait venir de l'espace amenées par des météorites, des poussières cométaires… Polymériser des molécules prébiotiques issues de l'espace ne pose pas de problème minéralogique : les argiles sont très fréquentes dans des milieux type mare côtière. Mais il se pose un problème de concentration des monomères dans ce genre de site, problème de concentration beaucoup plus ardu qu'au voisinage d'une source hydrothermale où il y a production continue de molécules organiques.
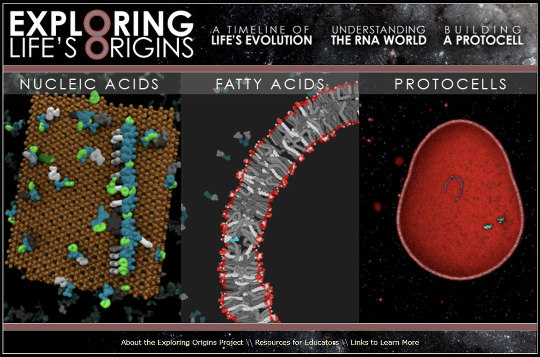
Une fois formés, ces polymères peuvent s'associer pour former des films organiques (les futures membranes), films qui peuvent se replier et former des agrégats appelés coacervat. Si ces polymères ont à la fois des capacités d'autoréplication et des capacités catalytiques, comme c'est le cas de l'ARN, on n'est pas loin de la vie. Mais on est là dans le domaine de la pure biochimie, et hors du champ de compétence des géologues. À défaut d'expliquer ces étapes cruciales dans cet article de sciences de la Terre, on peut l'illustrer. Une exposition virtuelle sur le thème Explorer l'origine de la vie, élaborée par la NSF (National Science Fondation) et le Musée des Sciences de Boston, est disponible sur le web. C'est une source de données, de schémas… dont est tirée la figure suivante et qui montre le type de recherches que mènent les biochimistes et les biologistes cellulaires.
Source - © 2013 ExploringOrigins
Sont illustrés la synthèse des polymères sur des surfaces minérales, la fabrication de membranes, avec utilisation d'acides gras, et l'apparition des premières cellules aussi simples soient-elles.
Croitre et multiplier
Une fois que les premiers unicellulaires dont nous descendons sont apparus, il a fallu qu'ils croissent et se multiplient, sinon cette vie primitive n'aurait été qu'un feu de paille. Il n'est d'ailleurs pas inenvisageable que plusieurs “vies” soient apparues vers −4 Ga, mais qu'une seule aient pu prospérer. Il existe deux métabolismes qui permettent aux organismes de vivre : l'hétérotrophie et l'autotrophie.
Source - © 2020 location-bessans.com
Figure 28. Autotrophes et hétérotrophes
Pour simplifier (en oubliant par exemple les symbioses…), il y a deux sortes d'organismes : les autotrophes et les hétérotrophes.
Les autotrophes absorbent H2O, CO2, sels minéraux et énergie pour faire leurs propres molécules, qui leur servent à grandir, à se reproduire, à produire l'énergie métabolique dans leurs cellules en les dégradant… Ici, c'est ce que fait l'herbe.
Les hétérotrophes, eux, absorbent des molécules toutes faites, molécules contenant carbone, azote…, molécules qui leur permettent de grandir, de se reproduire et de se fournir en énergie en les dégradant. Ici, c'est ce que fait la vache.
Les hétérotrophes, comme les animaux, les champignons, de nombreuses bactéries et archées actuels, tirent leur “substance” de molécules organiques “toutes faites” prises à l'extérieur et tirent l'énergie nécessaire à leur métabolisme en dégradant ces molécules par la respiration (si de l'O2 ou d'autres oxydants sont disponibles), ou par des fermentations… Or des molécules organiques sont présentes au niveau des sources hydrothermales car elles y sont synthétisées de façon abiotique. Ces molécules organiques sont à priori plus rares dans des sites de type mare côtière en l'absence d'autotrophes. En effet, la chute de poussières cométaires ou de météorites apportant ces molécules est quand même un phénomène peu fréquent à l'échelle d'une mare ou de la vie d'une cellule (même à l'époque) ; et si une cellule doit attendre la chute d'une météorite pour “manger“… Il y a donc à priori beaucoup moins de réactions exothermiques utilisables par une vie hétérotrophe dans des environnements de type mare côtière (anoxiques à l'époque) qu'au voisinage d'une source hydrothermale.
Les autotrophes, comme les végétaux et de nombreuses bactéries et archées actuels, synthétisent eux-mêmes ces molécules organiques grâce à du CO2, de l'H2O, des composés minéraux apportant azote, soufre, phosphore…, et un apport d'énergie extérieure pour réduire le CO2 et synthétiser des macromolécules. Cette énergie peut provenir de la lumière (photosynthèse sensu lato), ce que tout le monde connait. Mais cette énergie peut aussi provenir de réactions chimiques exothermiques dans le cas de ce qu'on appelle la chimiolithotrophie (cf. Les sources thermominérales d'Auvergne : chimiolithotrophie et photosynthèse). La chimiolithotrophie était très peu connue des non spécialistes avant 1977, année où elle est sortie du monde très restreint des microbiologistes. En effet, c'est en 1977 qu'on a découvert les sources hydrothermales du fond des océans et leurs prodigieux écosystèmes à priori indépendants de la photosynthèse. Depuis cette date, tout et n'importe quoi a été dit sur la source d'énergie à la base de ces écosystèmes hydrothermaux. Les sources d'énergie utilisées par les microorganismes à la base des chaines alimentaires de ces écosystèmes sont des réactions d'oxydo-réduction, alors que certains évoquaient la simple chaleur (ce qui violerait les principes de la thermodynamique), que d'autres proposaient le soufre, sans penser que dans une réaction d'oxydo-réduction, s'il faut un réducteur (ici le soufre), il faut aussi un oxydant, qui était passé sous silence. Dans la nature actuelle, les deux principales réactions d'oxydo-réduction utilisées par les microorganisme chimilithotrophes sont l'oxydation des sulfures et/ou du fer Fe2+ par le dioxygène dissout dans l'eau de mer : H2S + 2 O2 → H2SO4 et 4 FeO + O2 → 2 Fe2O3. Mais ces réactions ne sont possibles que parce que l'eau de mer est oxydante et contient beaucoup d'O2 dissout (les poissons respirent très bien dans l'eau de mer). Les écosystèmes des sources du fond des océans actuels dépendent donc (indirectement) de la photosynthèse, via le dioxygène dissout dans l'eau de mer. Il y a 4 Ga, la mer ne contenait pas d'O2 dissout et ce type de réaction ne pouvait pas avoir lieu. La majorité et les plus photogéniques des organismes des écosystèmes des sources hydrothermales océaniques classiques actuelles ne sont donc pas des équivalents de ce qui se passait il y a 4 Ga, contrairement à ce que disent nombre de médias et vulgarisateurs.
Mais, même aujourd'hui, il existe aussi des microorganismes chimiolithotrophes au niveau des sources hydrothermales utilisant des réactions chimiques sans intervention d'O2. C'est le cas en particuliers d'archées méthanogènes qui mettent en œuvre (par voie enzymatique) des réactions de type Sabatier (déjà vu à la partie Origine hydrothermale, mais il s'agissait de réactions abiotiques) en consommant l'H2 provenant des réactions de serpentinisation : 4 H2 + CO2 → CH4 + 2 H2O. Au niveau des sources hydrothermales sous-marines actuelles, il y a donc deux voies de production de méthane : une voie abiotique purement minérale, et une voie biologique grâce à des archées méthanogènes. Les parts respectives de ces deux voies restent à déterminer. Ce genre de chimiolithotrophie méthanogène pouvait vraisemblablement exister il y a 4 Ga.
Indépendamment du problème de la vie primitive, on peut remarquer que des archées méthanogènes existent dans des milieux très courants, bien moins “exotiques” que les sources hydrothermales sur péridotite. C'est le cas, par exemple, de ce qui se passe dans l'estomac (le rumen, pour être précis) des ruminants ou des termites, dans des vases anoxiques de marécages (dont les rizières) avec les feux follets… La chimiolithotrophie étant responsable d'une part non négligeable de l'émission des gaz à effet de serre, peut-être va-t-elle sortir de l'oubli dans lequel elle est actuellement cantonnée.
La seule autotrophie possible dans les obscures profondeurs marine est la chimiolithotrophie, en particulier au niveau des sources hydrothermales. Mais à faible profondeur (dans la zone photique), en plus de la chimiolithotrophie toujours possible, il y a la photosynthèse, ou plutôt les photosynthèses. Tout le monde connait la photosynthèse classique, oxygénique, où H2O est le donneur d'électron : CO2 + H2O + hν [photon] → C(H2O) [glucide] + O2. La signature géologique d'une telle photosynthèse serait un milieu très oxydé, donc possiblement riche en Fe2O3 (hématite).
On connait un peu moins la photosynthèse anoxygénique où H2O est “remplacé” par H2S comme donneur d'électron : CO2 + H2S + hν [photon] → C(H2O) [glucide] + S2. Cette photosynthèse (qu'on pourrait appeler sulfogénique bien que ce nom ne soit pas utilisé) est actuellement effectuée par certaines bactéries, comme les bactéries pourpres. La signature géologique d'une telle photosynthèse serait un milieu réduit, riche en soufre élémentaire.
Il existe un troisième type de photosynthèse, encore moins connu par les non spécialistes : la photoferrotrophie. Là, c'est du Fe2+ qui est le donneur d'électron, avec deux “variantes” possibles : CO2 + H2O + 4 FeO + hν [photon] → C(H2O) [glucide] + 2 Fe2O3 (hématite), ou, dans les milieux particulièrement riches en Fe2+ : CO2 + H2O + 6 FeO + hν [photon] → C(H2O) [glucide] + 2 Fe3O4 (magnétite). Ce type de photosynthèse est effectué actuellement par certains microorganismes dans des milieux anoxiques très riches en Fe2+. La signature géologique de cette troisième photosynthèse serait un milieu riche en magnétite.
Les environnements hydrothermaux superficiels (en zone photique) archéens et hadéens étaient bien sûr anoxiques et étaient théoriquement plus riches en Fe2+ que la pleine mer ou que des mares côtières de l'époque. La photosynthèse “sulfogénique” et la photoferrotrophie devaient être possibles. Dans les roches issues des plus vieux environnements volcano-sédimentaires âgés de 3,8 à 4 Ga, le soufre élémentaire est rarissime, mais les oxydes de fer sont abondants, comme dans les plus vieux fers rubanés qu'on trouve à Isua (Groenland), bien avant la grande oxygénation datée de 2,4 à 2,5 Ga. Et si les fers rubanés “récents” sont constitués d'hématite, les fers rubanés archéens anciens comme ceux d'Isua sont constitués très majoritairement de magnétite. Ces données de terrains ne suggèrent pas l'existence d'une photosynthèse sulfogénique mais indiqueraient l'existence d'une photoferrotrophie précoce à l'Archéen ancien.
Dans les environnements de type mare côtière sans source hydrothermale, à priori pauvres en fer réduit (ou en soufre), la photosynthèse oxygénique est la plus probable.
Cette autotrophie à l'Archéen ancien est également fortement suggérée par le fractionnement isotopique du carbone, par l'existence de stromatolites certaines à −3,5 Ga (Australie), et probables (mais discutées) à −3,8 Ga au Groenland.
Source - © 2019 - 2020, Blackwell Boyce, modifié — Pierre Thomas
Figure 30. Les fers rubanés de l'Archéen ancien à Isua, Groenland
Ces fers rubanés attirent un aimant (photo du bas à droite), preuve qu'ils contiennent de la magnétite (Fe3O4), contrairement aux fers rubanés les plus fréquents qui sont constitués d'hématite (Fe2O3), comme ceux, par exemple, de Barberton (Afrique du Sud) (cf. Les fers rubanés (Banded Iron Formation) de l'Archéen de Barberton, groupe de Fig Tree (−3,26 à −3,22 Ga), Afrique du Sud).
Conclusion et perspectives
Face aux quatre étapes théoriques proposées dans la troisième partie, il reste un problème encore loin d'être résolu : la troisième étape, à savoir le passage des macromolécules complexes à la plus simple des cellules. Les trois autres étapes posent moins de problèmes, même si rien n'est définitivement acquis. (1) Les molécules prébiotiques peuvent avoir deux origines, extraterrestre ou hydrothermale. (2) La polymérisation de ces molécules prébiotiques peut se faire en présence de phyllosilicates, phyllosilicates qu'on trouve au niveau des sources hydrothermales et de milieux argileux type mare côtière. (4) Le métabolisme des premières cellules pouvait être l'hétérotrophie au niveau des sources hydrothermales, l'autotrophie par photosynthèse en surface (mare côtière), l'autotrophie chimiolithotrophe au niveau des sources hydrothermales, et les deux types d'autotrophie, chimiolithotrophie et photosynthèses, au niveau des sources hydrothermales situées en zone photique.
Dans cette énumération d'environnements où a pu apparaitre et prospérer la vie, un type de site revient souvent, plus souvent que d'autres : les sources hydrothermales. Est-ce là qu'est née la vie ? Cela y est plus “facile” que dans d'autres environnements, qui ne sont pas pour autant exclus. Affaire à suivre !
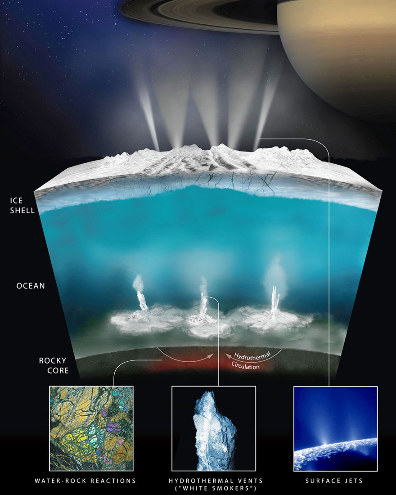
On peut enfin se demander où, dans le système solaire, ont pu être réunies les conditions permettant le commencement, voire la perpétuation de la vie. À part la Terre, deux types de corps réunissent ces conditions : Mars pendant son premier milliard d'années, et plus tard en contexte souterrain, et les corps glacés où de l'eau liquide est en contact avec des silicates : Europe, Encelade, Pluton…
Source - © 2017 NASA /JPL-Caltech /Southwest Research Institute
De haut en bas, on voit une banquise fracturée par où s'échappent des geysers, un océan d'eau maintenu liquide par la forte chaleur produite par les marées dans le noyau rocheux, et l'interface eau liquide /silicates avec sans doute des sources hydrothermales. Il y a tout ce qu'il faut pour qu'une vie y soit apparue et y existe encore. Il ne reste plus qu'à y aller voir !