Article | 17/05/2013
Le di-hydrogène naturel, une réelle source d'énergie ou un buzz médiatique ?
17/05/2013
Résumé
De l'hydrogène natif en Russie continentale : curiosité géologique ou réelle source énergétique exploitable ?
Table des matières
Un buzz médiatique
Figure 1. La recette pour faire de l'hydrogène à partir de fer réduit et d'eau
Recette chantée par le savant Cosinus pour endormir ses deux jumelles, Sécante et Cosécante.
D'après le scan d'un livre de P. Thomas, avec réécriture des légendes (sans modification du texte) pour plus de lisibilité.
Source : Le Petit Français illustré, journal des écoliers et des écolières, 561, Armand Colin et Cie éditeurs, 25 novembre 1899.
Fin avril / début mai 2013, il y a eu un buzz dans les milieux de l'énergie et dans la presse scientifique (on en a même parlé pendant un journal TV de 20h !) : « on » a trouvé des sources naturelles de di-hydrogène, possible ressource d'énergie renouvelable et non polluante. En France, « on » est principalement l'IFPEN (Institut Français du Pétrole, Énergie Nouvelle), source a priori sérieuse qu'il faut prendre en considération. Une copie d'écran de Google quand on tape « hydrogène naturel énergie » montre l'importance de ce buzz.
Avant de présenter rapidement cette information en insistant sur ses aspects géologiques, quelques mots sur l'hydrogène et son potentiel énergétique.
Hydrogène et potentiel énergétique
L'élément hydrogène (H) est le plus abondant des éléments de l'Univers (90% des atomes, environ 70% de la masse). Il est nettement moins abondant sur Terre, puisqu'il n'est principalement présent que dans l'eau (H2O), eau qui représente environ 10-3 de la masse de la Terre, que ce soit sous forme d'eau libre (océans et glaciers), d'eau circulant dans la croûte ou le manteau, ou d'eau dans les minéraux hydratés (amphiboles, serpentines, micas…). Mais ces 10-3 d'H2O représentent quand même plus de 1021 kg, soit environ 1020kg d'H sur Terre.
L'hydrogène est potentiellement une source d'énergie de deux manières fondamentalement différentes.
- Une source d'énergie chimique, la réaction du di-hydrogène moléculaire H2 avec du di-oxygène atmosphérique O2 (H2 + ½ O2 ➜ H2O) libérant de l'énergie (286 kJ.mol-1). Cette énergie peut être libérée sous forme de chaleur (cas de la combustion), ou sous forme électrique dans les « piles à combustible ».
- Une source d'énergie nucléaire grâce à la fusion (4H ➜ He, ou ses variantes avec les différents isotopes de l'hydrogène). C'est ce qui se passe dans les étoiles et dans les bombes "H". Mais on est encore très loin de savoir maîtriser cette fusion nucléaire de façon contrôlée, et on ne sait pas si on y arrivera un jour (projet ITER). Cette réaction de fusion libère environ 107 fois plus d'énergie par mole d'H2 que la réaction de combustion chimique.
C'est bien sûr l'énergie chimique (et non nucléaire) qui est évoquée quand on parle de l'hydrogène comme source d'énergie dans un avenir prévisible. Beaucoup de (mauvais) journalistes, commentateurs et écologistes parlent souvent d'une civilisation où l'hydrogène serait une source d'énergie presque inépuisable (puisqu'on trouve de l'hydrogène en quantité énorme -1020 kg !- dans l'océan), et non polluante puisque sa combustion ne génère que de l'H2O. Le problème, c'est que si l'atome H est abondant sur Terre (1020 kg !), la molécule H2 n'existe quasiment pas à l'état naturel sur Terre (sauf si les dernières nouvelles sont exactes). Avant de l'utiliser, il faut donc la produire.
La molécule H2 est abondamment synthétisée par l'industrie moderne qui en consomme de grandes quantités (synthèse de l'ammoniac utilisé dans les engrais, industrie des plastiques…). Mais la totalité de cet H2 est produit à partir de réactions endothermiques qui consomment beaucoup d'énergie et produisent du CO2. La majorité (96%) de l'H2 est produite à partir de charbon ou d'hydrocarbures par des réactions nommées « reformage catalytique », dont la plus fréquente peut être résumée par la formule :
- CH4 + 2 H2O + Énergie ➜ CO2 + 4 H2.
Cette réaction se fait à hautes température et pression (800°C et 20 atmosphères) et produit beaucoup de CO2 (celui produit par la réaction, et celui produit par la combustion du méthane nécessaire à maintenir le "réacteur" à 800°C et 20 atm. Utiliser cette H2 comme source d'énergie serait donc (1) non rentable énergétiquement parlant et (2) extrêmement polluant.
Environ 4% de l'H2 est obtenu par électrolyse de l'eau, réaction grande consommatrice d'énergie (elle en consomme plus que n'en fournit la combustion de l'hydrogène produit par ce procédé, le rendement énergétique global de l'ensemble électrolyse-combustion variant de 50 à 80%). Par contre, si cette production d'H2 par électrolyse n'est en aucun cas une source d'énergie, cela peut être un moyen de stocker l'énergie électrique, ce qui permettrait d'utiliser en continu de l'électricité produite de façon intermittente. Par exemple, un champ d'éoliennes utiliserait une partie de son électricité produite les jours venteux pour produire du di-hydrogène, qui serait utilisé pour produire de l'électricité les jours sans vent.
C'est cette absence de di-hydrogène moléculaire H2 à l'état naturel sur Terre qui faisait dire aux journalistes, commentateurs et écologistes sérieux que l'hydrogène n'était pas une source d'énergie, mais tout au plus un moyen de stockage (ou de transport) d'énergie. C'est pour cela que les nouvelles de fin avril / début mai 2013 sont intéressantes, posent force questions et demandent des précisions et compléments "géologiques".
Di-hydrogène naturel et fonds océaniques
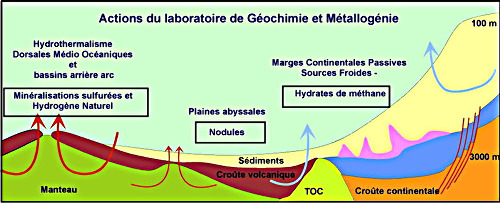
Le di-hydrogène naturel, encore appelé « hydrogène natif » était connu depuis un certain temps en particulier au niveau des sources hydrothermales océaniques, surtout celles jaillissant de fonds péridotitiques. On peut emprunter au site de l'Ifremer dans sa rubrique "géochimie" une figure et un texte.
Source - © 2011 Ifremer
On notera que la production de di-hydrogène (appélé ici « Hydrogène Naturel ») au niveau des dorsales est explicitement indiquée.
Ce même site (http://wwz.ifremer.fr/drogm/Activites/Geochimie#hydrogène) de l'Ifremer écrit ceci : « Hydrogène naturel. On se réfèrera sur ce sujet à l'article de Charlou et al., [2010], qui fait la synthèse comparative des différents sites ultramafiques d'activité hydrothermale découverts sur la dorsale Médio-Atlantique entre 12° et 40°N : Rainbow, 36°14'N ; Lost City, 30°N ; Logatchev l and II, 14°45'N ; Ashadze l and II, 12°58'N. L'analyse géochimique indique que les fluides hydrothermaux sont tous d'origine mantellique. Ils ont tous en commun des faibles concentrations en H2S et de fortes concentrations en H2, comparativement aux fluides prélevés dans des contextes basaltiques. La production d'hydrogène est donc directement liée au processus de serpentinisation. »
Quelles sont les réactions produisant cet hydrogène natif (H2) au niveau ou au voisinage des dorsales ? Il s'agit de l'action (à haute température) de l'eau sur l'oxyde ferreux (FeO), ce qui produit de la magnétite (Fe3O4) et du di-hydrogène :
- 3 FeO + H2O ➜ Fe3O4 + H2.
Le FeO libre n'est pas un minéral naturel, mais il est présent dans les silicates contenant du fer, comme la fayalite :
- 3 Fe2SiO4(fayalite) + 2 H2O ➜ 2 Fe3O4(magnétite) + 3 SiO2(silice) + 2H2.
La fayalite "pure" (pôle ferreux des olivines) est très rare dans la nature, mais l'olivine "usuelle" en contient environ 10%, pour 90% de forstérite (pôle magnésien des olivines).
La réaction de l'eau sur la forstérite produit de la serpentine et de l'hydroxyde de magnésiu :
- 2 Mg2SiO4(forstérite) + 3H2O ➜ Mg3Si2O5(OH)4(serpentine) + Mg(OH)2(brucite).
La réaction à haute température de l'eau sur l'olivine "usuelle", mélange de forstérite et de fayalite, peut donc s'écrire :
- olivine + eau ➜ serpentine + magnétite + brucite + di-hydrogène.
L'olivine est le minéral qui réagit le mieux avec l'eau et qui produit le plus de di-hydrogène. Mais tout minéral contenant du Fe2+ (pyroxène, amphibole, mica noir…) peut aussi réagir avec l'eau et donner de l'hydrogène natif.
On sait donc depuis 20 à 30 ans qu'il y a production continue de di-hydrogène au niveau des dorsales, en particulier celles où le manteau affleure ou est sub-affleurant. Mais le caractère dispersé (sur 60.000 km de long) et les difficultés d'une éventuelle exploitation de ce di-hydrogène naturel font que personne n'en envisageait l'exploitation à court ou moyen terme. « On » avait aussi prospecté rapidement cet hydrogène naturel au niveau des massifs péridotitiques émergés (principalement ophiolitiques), mais sans grand résultats.
J.L. Charlou, J.P. Donval, C. Konn, H. Ondréas, Y. Fouquet, P. Jean-Baptiste, E. Fourré, 2010. High production and fluxes of H2 and CH4 and evidence of abiotic hydrocarbon synthesis by serpentinization un ultramafic-hosted hydrothermal systems on Mid-Atlantic Ridge, In Rona P., Devey C., Dyment J. Murton B. Editors, “Diversity of hydrothermal systems on slow spreading ocean ridges”, Edited by AGU Geophysical monograph series 188, 265-296.
Di-hydrogène naturel en milieu continental
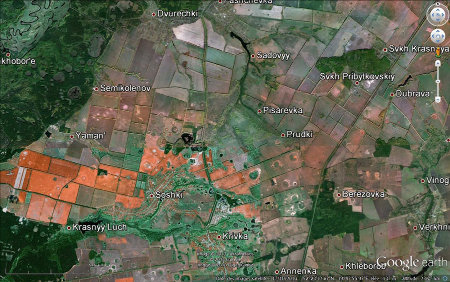
Ce qui a occasionné le buzz d'avril-mai 2013, c'est la découverte de dégagement de di-hydrogène au niveau de cratons (ou de plates-formes), en particulier en Russie. Sans revenir sur les péripéties qui ont suscité cette découverte et qu'on peut lire dans divers journaux (par exemple le blog scientifique de Libération), on peut résumer le communiqué de presse de l'IFPEN du 11 avril 2013 : il y aurait sous le bouclier russe (et sous d'autres boucliers) des réactions en profondeur ressemblant à celles qui se passent sous les dorsales ; des eaux chaudes réagiraient avec les minéraux ferro-magnésiens de roches basiques ou ultrabasiques, plus fréquentes dans la croûte des boucliers archéens que dans les autres parties des continents. On avait d'ailleurs déjà trouvé du di-hydrogène dans un bouclier, également en Russie : de l'hydrogène se trouvait en abondance dans les eaux et boues du forage de Kola, le plus profond du monde, effectué entre 1970 et 1989. Cet hydrogène généré en profondeur dans la croûte continentale serait plus ou moins canalisé par des fractures ou des roches poreuses, pourrait s'accumuler dans des aquifères poreux, et ressortir en surface. Les points de sorties se feraient souvent dans des dépressions circulaires peu profonde et de diamètre hectométrique ou kilométrique (appelées « trous de sorcière ») qui parsèment le bouclier et la plate-forme russe, dépressions dont l'origine reste à expliquer, mais qu'on voit très bien sur Google earth. Le di-hydrogène représente jusqu'à 80% des "fuites" au niveau des boucliers, le reste étant composé de méthane, parfois de di-azote, localement d'hélium.
Cette région est constituée d'un bouclier archéen recouvert de sédiments paléozoïques et mésozoïques.
D'autres origines pourraient être proposées pour expliquer ce dégagement de di-hydrogène, origines qui pour l'instant ne "tiennent pas la route" en fonction de ce qu'on connaît (ou croyons connaître) de notre planète et que nous ferons que citer sans les discuter : (1) dégazage continu de la Terre qui aurait piégé l'hydrogène de la nébuleuse solaire dans ses minéraux lors de sa formation ; (2) dégradation thermique d'hydrocarbures se transformant en graphite + di-hydrogène, ce qui expliquerait en partie la présence de méthane dilué dans l'hydrogène ; (3) décomposition de l'eau par les rayons γ issus de la désintégration des éléments radioactifs abondants dans les boucliers, ce qui expliquerait la présence d'hélium mélangé à l'hydrogène.
Des forages atteignant ces aquifères collecteurs de di-hydrogène, de la fracturation hydraulique (et oui, la revoilà !) dans des roches imperméables riches en di-hydrogène, des chiffres apparemment "astronomiques" (on trouve le chiffre de 40.000 m3/jour et par trou de sorcière, ce qui impressionne mais qui, tout compte fait, ne correspond qu'à 3,5 tonnes de di-hydrogène par jour) et bien d'autres informations/propositions difficilement vérifiables se trouvent sur le web.
Cet hydrogène natif continental est-il une réalité géologique massive et éventuellement exploitable, ou un simple phénomène géologiquement intéressant mais énergétiquement anecdotique ? L'avenir le dira. Ce qui est probable, c'est que si cette nouvelle s'avère réellement prometteuse en terme d'énergie, les informations réellement scientifiques se feront rares, les milieux pétroliers et assimilés ayant une culture du secret particulièrement exacerbée, concurrence oblige.
Conclusion
Comme il est en l'état difficile de conclure sur l'intérêt énergétique de cette information et sur les détails des mécanismes géologiques générant cet hydrogène et l'amenant en surface, on peut proposer en conclusion trois types de réflexions, réflexion sur les buzz médiatiques concernant la science, réflexion sur l'oubli puis la redécouverte de ce qui n'aurait jamais dû être oublié, réflexion sur l'importance géologique de la serpentinisation et autres réactions minérales voisines dont le di-hydrogène est un sous-produit.
Buzz scientifiques
Trois buzz médiatiques (sans l'amplification du web à l'époque) concernant la science ont eu lieu à la fin des années 1980 : la supraconductivité à "haute" température en 1986, la mémoire de l'eau en 1988, et la fusion froide en 1989. Sur ces trois "découvertes" totalement inattendues et révolutionnant la physique et la chimie, une seule s'est révélée exacte : la supraconductivité à haute température, source d'immenses progrès en physique théorique et de très nombreuses applications pratiques. L'hydrogène émis par les continents aura-t-il la destinée de la supraconductivité haute température ou celles de la fusion froide ou de la mémoire de l'eau tombées dans les oubliettes de l'histoire ?
L'oubli de la science de base
La production d'hydrogène au niveau des dorsales a été une relative surprise lors de sa découverte ; il en est de même de cette production dans les parties profondes des continents. Et pourtant ! La décomposition de l'eau par le fer réduit (fer métal ou fer2+) avec production de fer3+ et d'H2 est connue depuis au moins deux siècles, et pouvait l'être pas tous les « petits Français » de la fin du XIXème siècle. En témoigne l'une des premières bandes dessinées françaises, L'idée fixe du savant Cosinus, bande dessinée écrite entre 1893 et 1899 par Marie-Louis-Georges Colomb, qui signait ses œuvres sous le pseudonyme de Christophe. À la fin de ses aventures, Cosinus chante à ses deux filles (Sécante et Cosécante) la seule chanson qu'il connaissait : comment faire de l'hydrogène avec du fer et de l'eau (cf. figure 1). Si tous les géologues du XXème et XXIème siècles avaient lu et s'étaient souvenus des aventures du savant Cosinus... ou de leurs cours de chimie, ils auraient été moins surpris de cette production naturelle de di-hydrogène.
La serpentinisation
La serpentinisation et sa production de di-hydrogène associée est un processus géologique qui a peut-être changé la face du monde. En effet, ce di-hydrogène produit en profondeur peut réagir avec du CO2 qui, lui aussi, est présent en profondeur. À haute température, et à moins haute température en présence de catalyseur (et la magnétite est un de ces catalyseurs), H2 réagit avec le CO2 pour donner du méthane et d'autres hydrocarbures selon la réaction dite de type Fischer-Tropsch : 4 H2 + CO2 ➜ CH4 + 2 H2O. Si des composés azotés (N2, NH3…) sont également présents, ces synthèses peuvent aboutir à la formation de molécules complexes types acides aminés ou autres «« briques élémentaires » de la vie. Avec l'origine extra-terrestre via les météorites et comètes, la serpentinisation suivie de réaction de type Fischer-Tropsch est le deuxième mécanisme (non incompatible avec le premier) proposé pour l'origine des molécules prébiotiques sur Terre.
À plus basse température, dans des conditions compatibles avec la vie bactérienne (T < 120°C), cette réaction de type Fischer-Tropsch, exothermique, peut être le fait de bactéries dites méthanogènes. Ces bactéries effectuent cette réaction et utilisent l'énergie produite pour faire leur synthèse organique (chimiolithotrophie). Il existe ainsi de très nombreuses bactéries vivant dans le sous-sol profond, bactéries dites endogées, qui utilisent cette source d'énergie.
Quand on monte avec des élèves voir les ophiolites du Chenaillet à partir de Cervières, on marche longtemps sur des serpentinites. Si on passe un aimant puissant sur les produits d'altération (sable, terre…) liés à cette serpentine, on s'aperçoit que des petits grains de magnétite restent collés à l'aimant. Cette magnétite est, avec le di-hydrogène, un des sous-produits de la serpentinisation, possible mécanisme à l'origine de la vie sur Terre. Cela donne une autre ampleur au Chenaillet, qui n'est plus seulement une petite écaille ophiolitique issue d'un petit océan charrié sur une petite chaîne de montagnes, mais un témoin récent d'un processus majeur qui, il y a 4 Ga, a peut-être participé à l'origine de la vie.
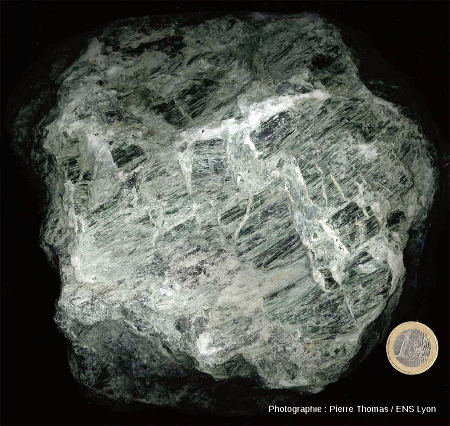
Figure 5. Échantillon de serpentinite
Cette roche est à considérer avec "respect" puisqu'elle est à l'origine de dégagements de di-hydrogène aussi bien océaniques que continentaux et qu'elle a peut-être participé à l'origine de la vie.