Image de la semaine | 27/04/2015
La fleur de sel, une forme cristalline de la halite (chlorure de sodium), lien avec les trémies et cubes de sel
27/04/2015
Résumé
Cristallisation du sel marin dans le système cubique, de la fleur de sel au gros sel, en passant par les trémies.
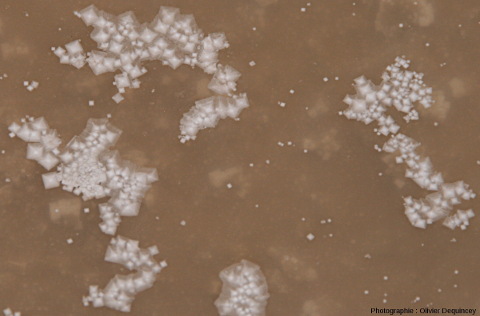
Figure 1. Cristal de fleur de sel (halite) de l'île de Ré vu au microscope optique
Ce cristal de fleur de sel a la forme d'une pyramide creuse (hopper crystal) (ici, sommet plat en avant, parois fines et transparentes) avec des parois à marches d'escaliers. La halite (chlorure de sodium) cristallise selon le système cubique.
Suite à des vacances à proximité de marais salants ou par goût pour la cuisine, vous connaissez certainement la fleur de sel. Ses petits cristaux pyramidaux et friables donnent un goût salé parfois particulier lorsque des algues s'y associent.
Le chlorure de sodium cristallise selon le système cubique. Dans les gisements de sel ou les salines (obtention de sel par évaporation de saumures), on trouve le sel sous forme de cubes "pleins" ("gros sel) ou de cubes à faces déprimées, les trémies (hopper cube). Dans une trémie de sel chaque face du cube ressemble à une pyramide creuse, avec sommet vers le centre du cristal. Une trémie peut donc apparaître comme l'adjonction de 6 pyramides pointant vers le centre du cube... On entrevoit ici une relation géométrique simple entre fleur de sel et trémie de sel.
Dans les marais salants, l'eau de mer débarrassée de ces impuretés et pré-concentrée lors d'étapes successives dans un circuit d'amenée de l'eau de mer, termine sa course dans de petits bassins appelés œillets dans lesquels a lieu la cristallisation puis la récolte du sel. Le sel marin "classique" se récolte après cristallisation lente sur le fond des bassins. Lors de journées particulières (air sec, chaleur, légère brise...) se forme, affleurant en surface, la fleur de sel qui est récoltée à part.
Nous vous montrons ici des photographies de sel prises au microscope, en vue rapprochée mais aussi sur des échantillons macroscopiques.
Figure 2. Cristal de fleur de sel (halite) de l'île de Ré Même cristal de fleur de sel que ci-dessus. S'il a bien la forme générale d'une pyramide on remarque qu'elle n'est pas parfaite, la face inférieure étant légèrement déformée (présence d'une arête supplémentaire... dont on voit la prolongation en arrière-plan). | Figure 3. Cristal de fleur de sel (halite) de l'île de Ré Ce cristal de fleur de sel a bien la forme générale d'une pyramide mais montre des croissances préférentielles selon certaines arêtes. |
Figure 4. Gros cristal de fleur de sel (halite) de l'île de Ré Sur ce cristal relativement symétrique de fleur de sel, on observe en haut à droite ce qui est soit une excroissance (point de nucléation en un coin de base de la pyramide) soit le résultat de l'accolement d'un plus petit cristal. En bas à droite, on remarque une croissance préférentielle prolongeant une arête de la pyramide principale. On voit aussi que la face de droite n'est pas plane puisqu'une arête supplémentaire est présente. La pyramide principale n'est donc pas "parfaite" mais a largement dominé la cristallisation de l'ensemble observé. | Figure 5. Cristaux imbriqués de fleur de sel (halite) de l'île de Ré Deux pyramides de fleur de sel sont enchevêtrées. La halite (chlorure de sodium) cristallise selon le système cubique. |
On peut aussi observer la forme pyramidale sur quelques "gros grains" de fleur de sel pris en photographie rapprochée.
Figure 6. Cristal de fleur de sel (halite) vu de profil On remarque que la pyramide repose sur une base "cubique" dont les arêtes se sont développées pour former les parois de la pyramide creuse. La distance entre les "dents" (ou les creux) de la pince servant d'échelle est de l'ordre du millimètre. | Figure 7. Vue de l'intérieur de la pyramide creuse d'un cristal de fleur de sel (halite) On voit bien, ici, que l'intérieur de la pyramide est creux. La distance entre les "dents" (ou les creux) de la pince servant d'échelle est de l'ordre du millimètre. |
Figure 8. Cristal de fleur de sel (halite) vu depuis le sommet de la pyramide La finesse des parois (transparentes) contraste avec l'épaisseur du sommet (opaque) de cette pyramide. La distance entre les "dents" (ou les creux) de la pince servant d'échelle est de l'ordre du millimètre. | |
Figure 9. Un marais salant de l'île de Ré Le sel mis en tas au premier plan est du sel en cube (voir plus bas), raclé sur le fond argileux de la placette. | |
Figure 11. Fleur de sel (halite) flottant à la surface de l'eau On voit bien, ici, les cristaux pyramidaux semblables aux vues des premières figures. | Figure 12. Fleur de sel (halite) flottant à la surface de l'eau On voit bien, ici, les cristaux pyramidaux semblables aux vues des premières figures. |
On trouve aussi dans la fleur de sel des cristaux un peu particuliers formés de deux pyramides partageant un même sommet.
Figure 13. Cristal de fleur de sel bipyramidé (halite) de l'île de Ré
On observe ici deux pyramides partageant le même sommet constitué d'une plaquette carrée.
Tout en gardant une forme pyramidale, on est donc passé d'une pyramide simple à une pyramide double. Si on imagine maintenant une base cubique, chaque face peut servir de départ à une pyramide. On a alors 6 pyramides creuses partageant leurs faces et pointant vers un même cube de départ. La forme obtenue, avec des pyramides équilibrées, est alors un cube à face creuses appelé trémie de sel.
Source - © 2010 Rob Lavinsky / iRocks.com sur wikimedia, CC-BY-SA-3.0 Figure 14. Trémies de halite, Searles Lake, Californie La halite est ici sous forme de cubes enchevêtrés à faces déprimées. | Source - © 2010 Rob Lavinsky / iRocks.com sur wikimedia, CC-BY-SA-3.0 Figure 15. Trémies de sel (halite), Saskatchewan, Canada On reconnaît bien les cubes de trémie de sel, mais certaines faces sont peu voire pas du tout déprimées... moindre "creusement" initial ou comblement secondaire. |
Le sel marin récolté au fond des œillets montre lui des formes cubiques plus classiques.
Figure 16. Cubes de sel (halite) de l'île de Ré vu au microscope optique Ces cristaux de sel accolés sont cubiques à faces "pleines". | Figure 17. Cubes de halite (chlorure de sodium) de l'île de Ré vus au microscope optique Ces cristaux de sel accolés sont cubiques à faces "pleines". |
Figure 18. Cube de sel marin de l'île de Ré La croissance du cristal semble s'être opérés par croissance des faces et non pas des arêtes du cube comme dans le cas des "pyramides", même si, ici, cette croissance semble commencer par les bords. La distance entre les "dents" (ou les creux) de la pince servant d'échelle est de l'ordre du millimètre. | Figure 19. "Gros" cube de sel marin de l'île de Ré La croissance du cristal semble s'être opérés par croissance des faces et non pas des arêtes du cube comme dans le cas des "pyramides". Ici, il semble même que cette croissance débute par le centre de la face avant 'étalement" vers les bords. La distance entre les "dents" (ou les creux) de la pince servant d'échelle est de l'ordre du millimètre. |
Dans les salines, l'obtention de trémies ou de cube résulte d'un choix (forme des récipients, température d'évaporation de la saumure...). Dans les marais salants, la cristallisation en fleur de sel ou en cubes correspond à deux contextes bien différents à partir d'eau de mer à quasi-saturation apportée dans les œillets.
Le fond des œillets est tapissé de cristaux de sel non récoltés reposant sur le fond argileux (une récolte complète endommagerait ce fond argileux imperméable). L'évaporation de l'eau aboutit à une lente saturation en chlorure de sodium. La cristallisation de halite peut se faire sur le support cristallin que constituent les cubes de sels non récoltés. La forme cubique se développe alors.
Lors de conditions météorologiques particulières, une forte évaporation permet la formation en surface d'une fine couche d'eau de mer sursaturée dans laquelle de fines plaquettes de sel peuvent se former. Ces plaquettes flottent à la surface du fait de tensions superficielles. Ces plaquettes sont soumises à leur poids, qui tend à les faire descendre dans la colonne d'eau, sont maintenues à la surface par les forces de tension superficielle, et baignent dans un milieu sursaturé en NaCl. Il apparaît que ces conditions (reproduites en laboratoire dans des expériences de cristallisation dans de minces films d'eau sursaturée) sont propices à la croissance cristalline par les bordures et les arêtes : la face supérieure est inaccessible car "à l'air libre" et la face inférieure est au contact d'eau un peu moins saturée). D'une plaquette, on passe donc à une plaquette entourée d'une bordure, formant une coupe tournée vers le haut. Cette coupe s'enfonce du fait de son poids mais est maintenue en surface du fait des tensions superficielles et de la flottabilité de l'édifice en construction, édifice qui peut cependant croître par les bords, d'où une forme pyramidale à quatre pans (les quatre côté du "cube" ou de la plaquette initiale) formant des marches d'escalier (croissance des parois par leur seul côté extérieur). Lorsque le poids des cristaux de fleur de sel devient trop important ou lorsque la pyramide se remplit d'eau (vaguelettes, pluie, augmentation de l'humidité de l'air en soirée...), les cristaux sédimentent au fond des bassins. Ils évoluent alors dans une saumure saturée (mais pas sursaturée comme en surface) jusqu'à la prochaine récolte du sel de fond : les pyramides servent alors de base à la cristallisation plus lente de la halite dans des conditions favorables au développement de cristaux cubiques "classiques".
Le fait de trouver des cristaux bipyramidés indiquent que la plaquette initiale peut parfois croître sur deux faces dans certaines conditions (épaisseur de la plaquette initiale, accolement de cristaux de fleur de sel qui modifient l'exposition du cristal à la saumure sursaturée, épaississement temporaire du film sursaturé... ?). Les trémies de sel "fossiles" et industrielles montrent qu'il est possible d'obtenir de gros cristaux et donc que des conditions particulières peuvent durer assez longtemps, et/ou que la croissance est interrompue avant remplissage des faces des trémies.
Source - © 2012 Damien Mollex / Lithothèque ENS de Lyon Figure 20. Cristaux de sel dans une argile La forme cubique des cristaux de sel est visible. | Source - © 2011 Damien Mollex / Lithothèque ENS de Lyon Figure 21. Sel, désert du Danakil, Éthiopie On devine les contours cubiques des cristaux de sel et on retrouve par endroits des traces de croissance en marche d'escalier (trémie de sel). |
Images diverses de halite à la page wikimedia:Halite.
Deux articles récents illustrés et documentés :
Dino Aquilano, Linda Pastero, Marco Bruno, Marco Rubbo, 2009. {100} and {111} forms of the NaCl crystals coexisting in growth from pure aqueous solution, Journal of Crystal Growth, 311, 2, 399-403
Pietro Fontana, Jürg Schefer, Donald Pettit, 2011. Characterization of sodium chloride crystals grown in microgravity, Journal of Crystal Growth, 324, 1, 207-211