Article | 06/03/2002
Le fractionnement de l'oxygène dans les nuages
06/03/2002
Résumé
Composition isotopique de l'oxygène dans les nuages et l'atmosphère et explication du calcul du δ18O.
Question
Objet : nuage Date : Lun, 17 Déc 2001 11:41:49 De : Michelle Barbier.
« Lorsqu'un nuage se déplace de l'Atlantique vers le Massif Central (par exemple), au fur et à mesure que la température diminue, le coefficient de fractionnement augmente. L'16O se concentre de plus en plus dans la vapeur et l'18O de plus en plus dans la phase liquide. Je voudrais savoir pour quelle température on a autant de 16O et de 18O ? est-ce possible dans la nature ? »
Réponse
Dans l'eau naturelle (océan, lac, vapeur, glace, etc), le rapport H218O/H216O est de l'ordre de 1/500 (0,002). Cette composition isotopique varie extrêmement peu, quelques pour-cents au plus, typiquement 1à 2% à nos latitudes, et jusqu'à 3-4% aux hautes latitudes. C'est pour cela que l'on utilise la notation δ (delta grec), qui permet d'exprimer de telles petites variations. On a choisi d'exprimer ces variations en ‰ et pas en pourcentages par commodité.
Ce δ est calculé comme suit :
ou "éch" représente l'échantillon d'eau dont on exprime la composition, par rapport à une référence "réf".
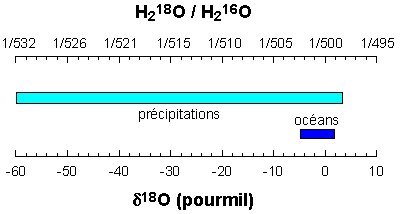
Figure 1. Composition isotopique des eaux naturelles
En haut, exprimée en rapport isotopique (nombre de molécules de H218O par rapport à H216O). En bas, composition exprimée en δ par rapport à la composition océanique moyenne de 1/500.
Les termes « appauvrissement » et « enrichissement » isotopiques se réfèrent toujours à ce rapport isotopique H218O/H216O. Dire que la pluie est « enrichie » par rapport à la vapeur du nuage veut dire exactement que son rapport H218O/H216O est plus élevé que celui de la vapeur. Mais ceci n'a rien à voir avec les quantités respectives de H218O et H216O : dans la pluie, il y aura toujours moins de H218O (et de H216O) que dans le nuage, puisque la pluie en provient et le rapport H218O/H216O est proche de 1/500 dans les deux cas.
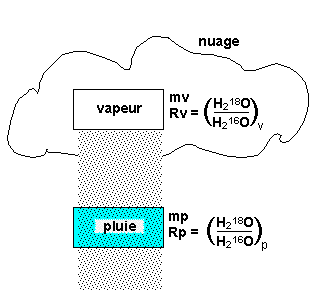
La masse de vapeur dans le nuage est "mV", très proche de la masse d'H216O, idem pour la masse "mP" de la pluie. La masse d'H218O dans la vapeur est mV x RV, dans la pluie mP x RP. La masse de pluie est plus faible que celle de vapeur dont elle provient, soit mV > mP (typiquement mP ~ 5 à 10% de mV). Les rapports isotopiques eux sont très proches : RV ~ RP ~ 1/500, mais à cause du fractionnement isotopique entre vapeur et liquide, on a strictement RV < RP (RV ~ 0,99 x RP). Les masses de H218O et H216O sont donc toujours plus grandes dans le nuage que dans les précipitations (mv > mp , et mv x Rv > mp x Rp), tandis que le rapport isotopique est toujours plus faible dans la vapeur que dans les précipitations (RV < RP).
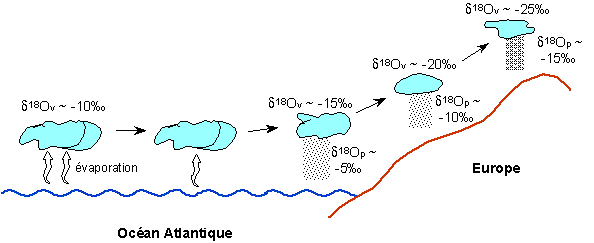
"L'appauvrissement isotopique" d'un nuage transporté de l'Atlantique vers le Massif Central (pour reprendre l'exemple), ne provient pas directement de l'effet de la température sur le fractionnement isotopique entre vapeur et précipitations. En effet, ce fractionnement est relativement constant : il passe de 10‰ à 25°C à 14‰ à -20°C. L'appauvrissement provient de l'épuisement en vapeur du nuage à cause des précipitations successives.
Notez la différence de 10‰ entre la composition isotopique de la vapeur et des précipitations, due au fractionnement isotopique.