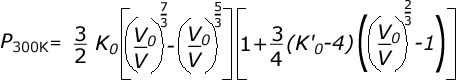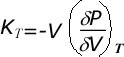Article | 27/09/2004
La cellule à enclumes de diamant
27/09/2004
Résumé
La cellule à enclumes de diamant, un instrument fondamental pour l'étude expérimentale des matériaux du manteau et du noyau terrestre, principe et applications.
Table des matières
- Introduction
- Le principe de l'appareil
- La préparation d'une expérience
- Quelques images de cellules à enclumes de diamants
- Le choix du milieu de transmission de la pression
- Mesurer la pression en cellule diamant
- Chauffer un échantillon dans une cellule de diamants
- Domaines d'application de la cellule à enclumes de diamant.
- Les laboratoires où cette technique est utilisée pour des applications en Sciences de l'Univers
Introduction
La cellule à enclumes de diamant est un instrument fondamental pour l'étude expérimentale des matériaux du manteau et du noyau terrestre. Le domaine de pression et température accessible par cette technique couvre pratiquement tout le domaine de pression et de température que l'on rencontre à l'intérieur de la Terre et des planètes telluriques : pression jusqu'à 500 GPa (5 millions d'atmosphères) et température jusqu'à 5 000 K. La transparence du diamant sur une large bande de longueur d'onde, de l'infrarouge aux rayons X et gamma permet de mesurer in-situ les propriétés des matériaux à haute pression et température variable.
Le principe de l'appareil
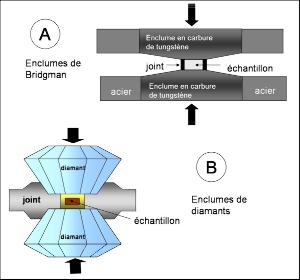
La cellule à enclumes de diamant repose sur un principe physique simple : pour atteindre des pressions élevées il faut appliquer une force importante sur une surface la plus réduite possible. Le diamant présente des caractéristiques de résistance à la compression exceptionnelles. C'est à la fin des années 1950 qu'un américain a eu l'idée d'utiliser des diamants comme enclumes dans un montage de type « presse de Bridgman » (Figure 1A). L'échantillon à étudier sous pression est placé dans un trou (de 50 à 300 mm de diamètre) percé dans une feuille de d'acier de quelques dixièmes de millimètres d'épaisseur que l'on serre entre deux diamants (Figure 1B).
L'échantillon à étudier sous pression est placé dans un trou (de 50 à 300 mm de diamètre) percé dans une feuille d'acier (le joint) de quelques dixièmes de millimètres d'épaisseur que l'on serre entre deux diamants.
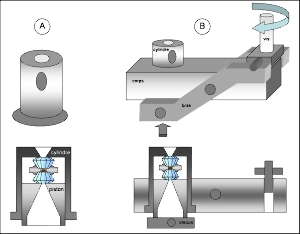
Les deux diamants sont taillés et présentent une surface plane (la tablette) d'un diamètre variant de 10 à 700 μm (voire plus). Pour être poussés en opposition les deux diamants sont placés respectivement sur un cylindre et un piston coulissant l'un dans l'autre (Figure 2). Le piston est poussé à l'aide d'un système mécanique qui la plupart du temps consiste en un système de levier et de vis manœuvré à la main (Figure 2). Il existe des systèmes pneumatiques plus sophistiqués permettant des mouvements contrôlés et fins de coulissage du piston dans le cylindre.
La préparation d'une expérience
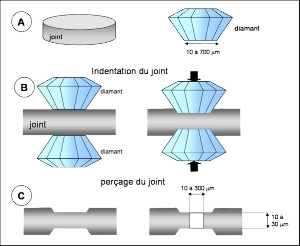
Les figures ci-dessous décrivent les étapes de préparation d'une expérience en cellule à enclumes de diamant. La première étape est la préparation du joint qui servira à confiner l'échantillon entre les deux diamants (Figure 3). On part d'un disque métallique d'environ 200 μm d'épaisseur et de quelques millimètres de diamètre. Ce disque est comprimé entre les deux diamants pour former une empreinte circulaire des tablettes. Un trou est ensuite percé au centre de cette empreinte. Le perçage se fait à l'aide de micro forets ou par électro-érosion. Le diamètre de l'empreinte et donc le diamètre des tablettes, l'épaisseur de l'empreinte et la taille du trou sont choisis en fonction de la pression maximale que l'on veut atteindre pendant l'expérience. Les tailles typiques varient dans les gammes suivantes :
- Epaisseur de l'empreinte : 10 à 30 μm
- Diamètres des tablettes des diamants : 10 à 700 μm
- Diamètre du trou : 10 à 300 μm
Figure 3. Préparation du joint métallique pour une expérience en cellule à enclumes de diamant.
A : Disque métallique de quelques centaines de microns d'épaisseur. B : indentation du joint et formation d'une empreinte des diamants. C : perçage d'un trou au centre de l'empreinte.
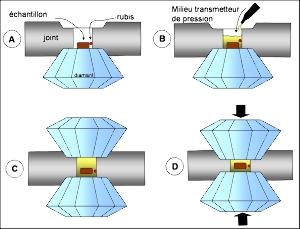
Cette première étape réalisée, on passe à la mise en place de l'échantillon (Figure 4). Le joint troué est positionné sur l'un des diamants et le minéral à étudier placé dans le trou. On ajoute ensuite des éclats de rubis (A), on remplit le reste du trou avec un milieu transmetteur de pression (liquides organiques, gaz rares, solides mous) (B) et on comprime l'ensemble entre les deux diamants (C). L'augmentation de la pression est induite par la réduction du volume du trou (D). Dans certains cas on ne remplit le trou qu'avec l'échantillon sans mettre de milieu transmetteur de pression.
Figure 4. Principes de chargement d'une cellule à enclumes de diamant.
A : mise en place du joint percé sur la tablette d'un diamant, positionnement de l'échantillon à étudier et d'un grain de rubis utilisé pour mesurer la pression. B : remplissage du trou avec un milieu (solide ou liquide) servant de transmetteur de pression à l'échantillon. C : mise en place du second diamant. D : compression par mouvement des diamants l'un vers l'autre.
Quelques images de cellules à enclumes de diamants
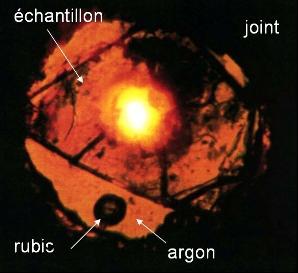
Figure 7. Vue de l'intérieur d'une cellule diamant.
On observe les deux diamants taillés en pointe comprimant le joint métallique.
Le milieu de compression est ici de l'argon. Un grain de rubis est situé en bas à droite.
Le choix du milieu de transmission de la pression
Le choix du milieu de transmission de la pression avec lequel on remplit le trou du joint est crucial. Pour que la pression soit la plus hydrostatique possible (i.e. qu'elle ait la même valeur en tous points du milieu) l'idéal est d'utiliser un liquide ou un solide mou. Les milieux les plus fréquemment utilisés sont :
- des mélanges d'alcools. Ils se transforment tous en solides pour des pressions de quelques GPa.
- des solides ioniques de type NaCl
- des gaz rares (Ar, Ne, He …). Ces derniers se transforment en solide mous pour de faibles pressions (quelques GPa) mais procurent des conditions de pression très hydrostatiques jusqu'à plusieurs centaines de GPa.
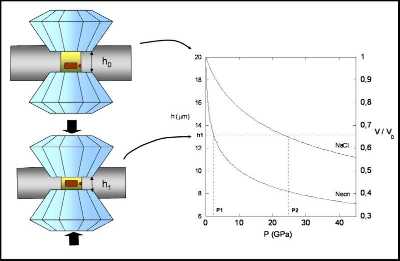
Pour mieux comprendre l'augmentation de la pression sur l'échantillon, regardons le schéma ci-dessous (Figure 9). Lors du mouvement des diamants l'un vers l'autre, le volume du trou diminue. Cette diminution est surtout liée à la réduction de la hauteur du trou. En effet, le diamètre de ce dernier ne change pas, ou du moins peu, si l'expérience est bien montée. Pour cerner le problème nous ferons l'hypothèse que le diamètre du trou reste constant et que seule son épaisseur diminue. Le volume initial(V0) du trou vaut :
V0 = h0.S0
où h0 est la hauteur initiale du trou et S0, la surface de la section du trou cylindrique. Après compression et diminution de la hauteur du trou de h0 à h, le volume vaut :
V = h.S0
Dans ce cas on remarque que la variation de volume V/V0 est la même que h/h0 :
V/V0 = h/h0
Le fluide ou le solide remplissant le trou subit la diminution de volume et se comprime. La pression augmente d'autant plus rapidement que le fluide ou le solide est peu compressible. Deux cas sont représentés sur le graphe de droite pour deux milieux de compressibilités différentes : NaCl et le néon. Sur l'ordonnée de droite on trouve la variation du volume V/V0. Cette variation est aussi celle du volume molaire ou du volume molaire du milieu qui remplit le trou. L'ordonnée de gauche exprime la variation de la hauteur du trou d'épaisseur initiale 20 μm. L'abscisse donne les variations de pression exprimée en gigapascals (GPa), 1 GPa = 109 Pa. La courbe correspondant à NaCl donne les variations V/V0 du volume molaire de ce solide en fonction de la pression. Quand le trou est réduit à une épaisseur de 13 μm, la pression dans NaCl est de P2 = 25 GPa. Le néon, solide à température ambiante à partir de 4 GPa, est nettement moins compressible que NaCl. On observe que pour une épaisseur de 13 μm la pression dans ce milieu n'est que de 2 GPa. Pour obtenir une pression de 25 GPa, il faut réduire l'épaisseur du joint à environ 8 μm.
Mesurer la pression en cellule diamant
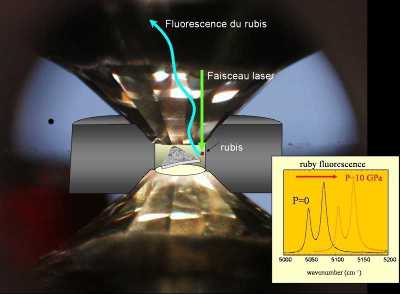
Les éclats de rubis servent à mesurer la pression à laquelle est soumise l'échantillon (Figure 5). Les rubis dopés avec des ions Cr3+ émettent une fluorescence quand ils sont éclairés par un faisceau laser. Cette fluorescence est analysée par un spectromètre. Le spectre montre deux raies de fluorescence qui se décalent avec la pression. Le décalage est calibré en fonction de la pression.
Figure 10. Coupe schématique d'une cellule à enclumes de diamants.
On voit les deux diamants, le joint circulaire, l'échantillon entouré d'un milieu transmetteur de pression et un éclat de rubis. La fluorescence de ce rubis due à des ions Cr3+ est excitée par un faisceau laser. L'encart en bas à droite montre le décalage des raies de fluorescence avec la pression.
Chauffer un échantillon dans une cellule de diamants
L'échantillon sous pression est chauffé par des fours résistifs entourant les diamants (pour des températures inférieures à 1 500 K) ou par focalisation du faisceau d'un laser IR de puissance (YAG ou CO2) pour atteindre des températures de l'ordre de 4 000 K.
Chauffage par four
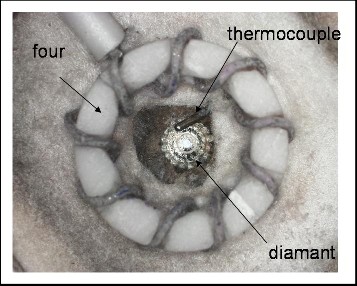
La figure 11 schématise le principe. Un micro four fait d'un bobinage de fil résistif entoure les diamants. La transformation du diamant en graphite limite la température à environ 1 500 K. Avec des montages particuliers (enceintes à atmosphères contrôlées ou des joints chauffants) on peut atteindre des températures plus élevées de l'ordre de 2 000 K. La température est mesurée par un thermocouple situé au contact des diamants.
Figure 11. Microfour résistif entourant les diamants.
Figure 12. Photographie d'un micro-four résistif entourant un diamant.
Le fil chauffant est bobiné autour d'un anneau en céramique. Un thermocouple au voisinage du diamant sert à mesurer la température.
Chauffage laser
Le diamant est transparent à une grande partie du spectre électromagnétique. Il l'est en particulier dans le domaine de la lumière infrarouge (IR), ce qui permet de focaliser sur des échantillons comprimés des faisceaux de laser de puissance IR (Figure 13 et 14). La plupart des oxydes ou métaux absorbent en revanche la lumière IR et s'échauffent. Cette technique permet donc de chauffer à plusieurs milliers de degrés les échantillons sans trop échauffer les diamants. La température est déduite de l'analyse de la lumière émise par l'échantillon chauffé. En effet, la couleur ou encore la distribution des intensités en fonction de la longueur d'onde de ce rayonnement dépend de la température à laquelle l'échantillon est porté (Figure 16).
Figure 13. Schéma de principe du chauffage d'un échantillon comprimé en cellule à enclumes diamant.
(1) Un faisceau laser infrarouge passe au travers de l'un des diamant spécialement sélectionné pour être transparent aux longueurs d'ondes de la lumière infra rouge. (2) La tache jaune correspond au point d'impact du faisceau laser qui échauffe l'échantillon à plusieurs milliers de degrés. (3) L'échantillon échauffé émet un rayonnement. L'analyse de ce dernier permet d'estimer la température à laquelle l'échantillon est porté.
Figure 14. Banc de chauffage laser pour cellule à enclumes de diamant.
Un laser de type CO2 (1) émet un faisceau infrarouge (2) qui par un jeu de miroirs (m) est amené dans une lentille (3) qui focalise le faisceau sur l'échantillon comprimé dans une cellule diamant (4). Un microscope (6) permet d'observer l'échantillon (Figure 15) et d'analyser à l'aide de spectromètres la fluorescence du rubis pour mesurer la pression (Figure 10) et le rayonnement émis par la zone chaude de l'échantillon (Figure 16) pour estimer la température.
Figure 15. Vue au travers d'un microscope d'un échantillon de quartz comprimé à 20 GPa entre deux diamants.
Le milieu de transmission de la pression est de l'argon. On voit aussi un grain de rubis servant à mesurer la pression. La tache jaune au centre de l'échantillon correspond à la zone chauffée par le faisceau d'un laser de puissance infrarouge passant au travers de l'un des diamants et absorbé par l'échantillon.
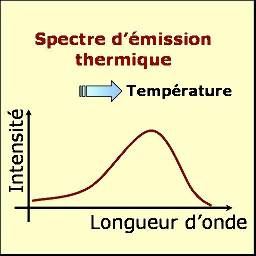
Figure 16. Spectre d'émission thermique.
Le rayonnement émis par la partie chauffée de l'échantillon (Figure 15) est analysé par un spectromètre et fournit une courbe de l'intensité de ce rayonnement en fonction de la longueur d'onde. Cette courbe peut être ajustée sur une loi d'émission de type corps noir et donner la température de l'échantillon.
Domaines d'application de la cellule à enclumes de diamant.
Les domaines d'application de la technique de la cellule à enclumes de diamant sont variés, depuis la physique des matériaux sous conditions extrêmes jusqu'à la géophysique en passant par la biologie ! La technique a donc beaucoup évolué pour permettre de comprimer en chauffant ou en refroidissant des matériaux solides ou liquides (magmas, minéraux, molécules organiques, éléments …). Le schéma ci-dessous illustre les différents champs de pression et de température accessibles par la cellule à enclumes de diamant.
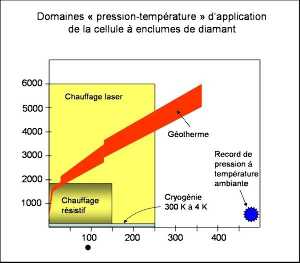
Figure 17. Les différents domaines « pression-température » d'application de la cellule à enclumes de diamant.
La cryiogénie sou pression se réalise en enfermant la cellule diamant dans un cryostat. La pression maximale obtenue en cellule diamant à température ambiante se situe aux alentours de 500 GPa ! Un géotherme permet de voir qu'une grnade partie des conditions de pression et de température caractéristiques de la Terre sont accessible à cette technique.
Que peut-on faire avec une cellule diamant ?
Avec une cellule à enclumes de diamant on peut réaliser une grande variété d'expériences. La transparence du diamant sur une large bande de longueur d'onde, de l'infrarouge aux rayons X et gamma permet en effet de suivre in-situ les changements que subissent les matériaux à haute pression et température. Il est donc possible de suivre le comportement des roches et minéraux et de préciser entre autre :
- les changements de densité (ou de volume molaire) en fonction de la pression et de la température,
- les changements de phases des minéraux,
- les variations des propriétés élastiques et de vitesses de propagation des ondes acoustiques en fonction de la pression et de la température
- les phénomènes de fusion à haute pression.
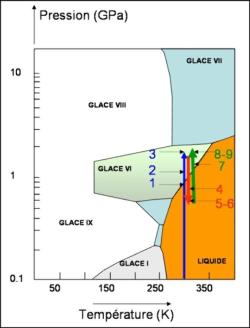
Un exemple visuel simple : les changements de phase de l'eau
Si, à la pression atmosphérique, on abaisse la température en dessous de 0°C, l'eau liquide se transforme en glace : la structure tétraédrique présente dans l'eau liquide se fige alors et l'ordre local devient un ordre à grande distance. Cette glace est un solide cristallin et c'est la glace commune que nous connaissons tous.
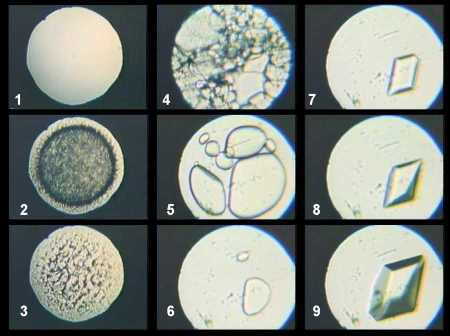
Mais il existe plein d'autres formes cristallines de glace que l'on obtient en comprimant une goutte d'eau dans une cellule à enclumes de diamant et cela à température ambiante. La Figure 18 montre une séquence de photographies prises au travers des diamants lors de la compression et de la décompression d'une goutte d'eau. Le schéma de la Figure 19 donne en coupe le déroulement de l'expérience. Chacune des photographies est repérée dans le diagramme de phase de H2O en Figure 20. Lors de cette expérience l'eau passe de l'état liquide à une forme solide cristallisée : la glace VI. Après avoir formé au-delà de 0,9 GPa un polycristal de glace VI, on décomprime la cellule de telle manière à faire coexister un seul cristal de glace VI avec l'eau liquide. En augmentant à nouveau lentement la pression au dessus de 0,9 GPa, on arrive à faire pousser un cristal unique de glace VI.
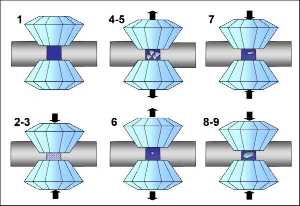
Les numéros des photographies sont localisés sur le diagramme de phase de H2O présenté dans la figure 20. La figure 19 présente des schémas en coupe de l'expérience. (1) : goutte d'eau enfermée dans le joint métallique et comprimée entre les deux diamants. (2) et (3) : lorsque les conditions de pression sont supérieures à 9 GPa (9 000 bars) l'eau se transforme en une multitude de cristaux de glace VI. (4), (5) et (6) : lorsque l'on diminue la pression en dessous de 0,9 GPa, la glace VI fond. Sur la photographie 6 il ne reste plus que deux cristaux de glace VI entourés d'eau liquide. (7), (8) et (9) : en réaugmentant lentement la pression au dessus de 0,9 GPa l'un des cristaux croît en développant de magnifiques faces cristallines.
Les numéros correspondent à ceux de la figure 18.
L'eau liquide correspond au champ orange. La glace standard (glace I) est stable dans le champ gris et la glace VI dans le champ vert. Lors de l'expérience décrite dans les figures 18 et 19 la température est fixe et égale à la température ambiante et la pression varie le long des différentes flèches verticales.
Un exemple visuel simple : la fusion de l'olivine à haute pression
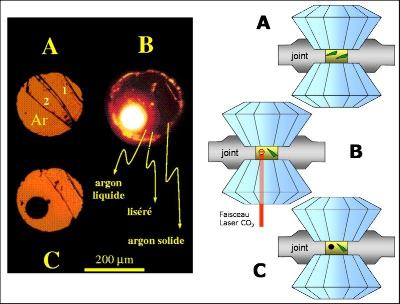
Déterminer la température de fusion d'un minéral ou d'une roche est essentiel pour comprendre les phénomènes magmatiques. A pression ambiante l'expérience est relativement aisée ; elle est plus difficile à haute pression. La cellule à enclumes de diamant permet de réaliser des expériences de fusion et cela jusqu'à des pressions de plusieurs dizaines de GPa. La figure ci-dessous (Figure 21) montre la fusion de cristaux d'olivine. Deux cristaux (1 et 2) sont comprimés avec de l'argon comme milieu de transmission de la pression. Le faisceau d'un laser IR de puissance est focalisé sur l'un des échantillons au travers de l'un des diamants. On augmente la puissance du laser jusqu'à induire la fusion (au environ de 2 500 K) qui se matérialise dans cette expérience par la formation d'une boule d'olivine fondue. En coupant le laser instantanément la température de l'échantillon redescend à la température ambiante en une fraction de seconde conduisant à une trempe du liquide en verre.
A : deux cristaux d'olivine (1 et 2) de 15 mm d'épaisseur sont comprimés dans de l'argon à 15 GPa. B : Le faisceau d'un laser IR de puissance est focalisé sur l'un des échantillons (le 2) au travers de l'un des diamants et forme une bille d'olivine fondue. La température est de l'ordre de 2 500 K. C : lors de la coupure du faisceau laser la température redescend à la température ambiante en une fraction de seconde conduisant à une trempe du liquide en verre. Les schémas de droite montrent les différentes étapes de l'expérience en coupe.
Rayons X et cellule à enclumes de diamant.
Les anneaux synchrotrons (tels que l'ESRF à Grenoble) permettent de générer des faisceaux de rayons X (RX) de quelques micromètres de diamètre, avec beaucoup de flux, collimatés ou focalisés, qui sont particulièrement bien adaptés aux expériences de haute pression en cellule à enclumes de diamant. Plusieurs types d'expériences sont envisageables avec les RX :
- diffraction des RX : études des structures des matériaux et de leurs changements avec la pression et la température ; mesures de compressibilité et de dilatation thermique ; texture et orientations préférentielles.
- absorption et fluorescence X : étude des compositions chimiques et des environnements atomiques.
La diffraction des RX : principes et montage
Les figures ci-dessous illustrent les principes d'une expérience de diffraction des RX en cellule à enclumes de diamant :
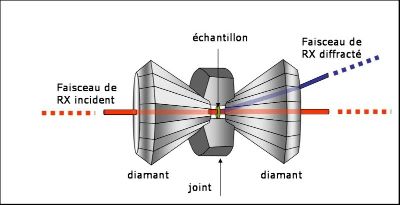
Figure 22. Schéma de principe d'une expérience de diffraction des RX en cellule à enclume de diamant. Le rayonnement incident est généralement transmis au travers du diamant « arrière » jusqu'à l'échantillon qui diffracte alors au travers du diamant situé entre lui et le détecteur. L'échantillon est soit une poudre ou un monocristal. | Figure 23. Un montage réel. |
Figure 25. Montage d'une cellule diamant sur une source de RX du synchrotron de LURE (Orsay). Le faisceau de RX incident (en rouge) passe dans la cellule diamant (voir figure 20) et est diffracté par l'échantillon comprimé entre les diamants (faisceau bleu). Le rayonnement X diffracté est collecté sur un détecteur. Source : Philippe Gillet. |
Les spectres de diffraction donnant les distances entre plans atomiques du minéral, cette technique permet de suivre in situ, à haute pression et température, les changements de phase des minéraux mais aussi comme nous allons le voir les variations de volume et donc de densité des minéraux en fonction de la pression et de la température.
Équations d'états des minéraux
Une équation d'état d'un matériau est une relation qui décrit les relations entre les grandeurs thermodynamiques pression-température-volume. Pour les gaz par exemple cette relation prend la forme :
PV=R T
Pour les solides elle est souvent exprimée sous la forme de l'équation de Birch-Murnaghan. A température ambiante cette équation s'écrit :
V0 est le volume à pression ambiante et 300 K et V le volume à la pression P et à la température de 300 K. K0 est le module d'incompressibilité à pression et température ambiante. Il représente une mesure de la résistance d'un matériau à la compression et s'exprime par
Comme les matériaux ne sont pas infiniment compressibles ce module augmente avec la pression et on définit K' par :
Pour les minéraux les paramètres de l'équation d'état à température T0 à déterminer sont KT et K'T< à partir de différents couples (P,V).
P et V sont mesurables en utilisant la cellule diamant couplée à des techniques de diffraction des RX. Les spectres de diffraction donnant les distances entre plans atomiques du minéral, on en déduit le volume molaire et si on fait l'expérience à différentes pressions on obtient la courbe de variation du volume en fonction de la pression.
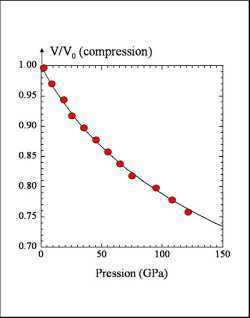
Figure 26. Courbe de compression de MgSiO3-perovskite.
Les expériences de compression en cellule à enclumes de diamant ont été réalisées à température ambiante. V0 est le volume du minéral à pression et température ambiantes. A partir de cette courbe on déduit la valeur du module d'incompressibilité et sa dérivée (KT et K'T).
Spectroscopie des vibrations en cellule à enclumes de diamant : exemple de la spectroscopie Raman à haute pression
Les spectroscopie Raman et infra-rouge sondent les vibrations au sein des cristaux, liquides et verres. Un spectre Raman ou infra rouge est constitué de pics (ou raies) qui donnent les fréquences de ces vibrations. Le nombre de vibrations, donc de pics, est déterminé par la symétrie du matériau. Les modifications des spectres au cours d'une transition de phase induites par la pression et par la température sont interprétables en termes de changements dans l'agencement des atomes (changements de coordinence) et de mouvements des atomes (mécanismes de changements de phase). Il est donc possible, toujours en couplant des cellules à enclumes de diamant et des platines chauffantes à un spectromètre Raman ou infra-rouge d'étudier in-situ à haute pression et température la dynamique des transitions de phase dans les matériaux. Dans ce qui suit, nous présentons les principes de la spectroscopie Raman à haute pression.
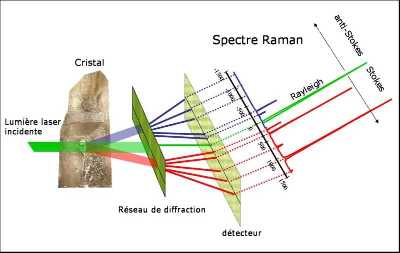
L'effet Raman peut être schématisé de la manière suivante (Figure 25). Un cristal est éclairé par un faisceau de lumière monochromatique. Une partie de cette lumière incidente est diffusée par l'échantillon. Si on analyse cette dernière par un système de réseau et de détecteur de type CCD on observe que la lumière incidente après interaction avec le cristal a perdu ou gagné de l'énergie.
Figure 27. Principe de l'effet Raman.
Ceci se traduit par un spectre présentant des pics (Raies Stockes et anti-Stockes). Ces gains ou pertes d'énergie résultent de l'interaction de la lumière incidente avec les vibrations des atomes dans le matériau. Ils sont caractéristiques du matériau et en sont en quelque sorte une fiche d'identité. Dans les montages modernes on utilise souvent des spectromètres Raman équipés de microscopes optiques qui permettent à la fois de focaliser un faisceau laser incident sur l'échantillon et à collecter la le rayonnement Raman (Figure 26). Les diamants étant transparents à la lumière visible on peut utiliser la cellule à enclumes de diamants pour réaliser des mesures de spectroscopie Raman à haute pression et haute température (Figure 26).
Figure 28. Montage d'une cellule à enclumes de diamant sur un spectromètre Raman.
L'encart donne le détail à l'échelle des diamants des différents trajets optiques entre l'échantillon comprimé et le spectromètre.
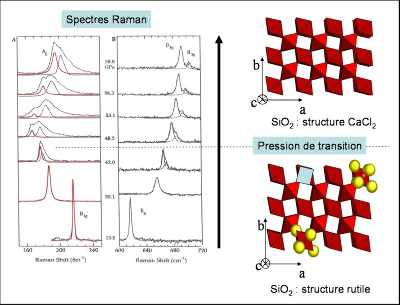
La figure ci-dessous (Figure 27) donne l'exemple de la transition de phase que subit à haute pression la stishovite, une forme cristalline de la silice SiO2. Cette transition s'observe en comprimant en cellule à enclumes de diamant à température ambiante et au-delà de 40 GPa des cristaux de stishovite. Lors de cette transformation, la stishovite, de structure rutile, adopte la structure du chlorure de calcium. Les spectres Raman enregistrés pendant toute la compression changent en réponse aux changements de l'agencement des atomes. On observe en particulier, l'apparition de nouveaux pics au-delà de 40 GPa.
On observe, au-delà de 40 GPa, le dédoublement du pic de basse fréquence (B1g) qui traduit le passage d'une structure de type rutile à une structure de type CaCl2.
Les laboratoires où cette technique est utilisée pour des applications en Sciences de l'Univers
Laboratoire de Minéralogie et cristallographie de Paris UMR CNRS 75690