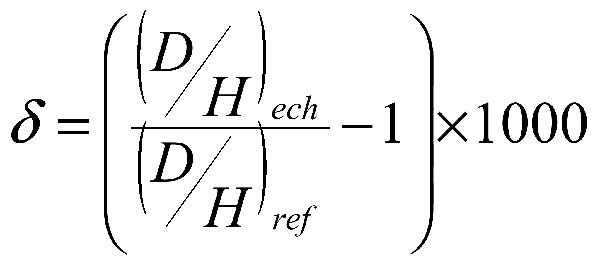Article | 08/02/2007
La matière organique dans les chondrites carbonées
08/02/2007
Résumé
Travaux de recherche entrepris depuis une trentaine d'années par différentes équipes dans le monde sur la matière organique dans les chondrites carbonées.
Table des matières
L'auteur remercie chaleureusement Sylvie Derenne, Jean-Noël Rouzaud et François Robert pour leurs commentaires et corrections.
Rappel historique
On connaît la présence de matière organique dans les météorites et notamment les chondrites carbonées depuis le milieu du XIXème siècle et les travaux de Berzelius. La chute de la météorite d'Orgueil, dans le Tarn-et-Garonne, en 1864 va permettre la mise en évidence d'une substance macromoléculaire organique proche des charbons terrestres d'après Berthelot. L'intérêt pour la matière organique des météorites revient vers 1950 avec l'amélioration des techniques analytiques. C'est à ce moment là que les premiers acides aminés sont mis en évidence. Mais très vite il s'avère que ces derniers sont des contaminants terrestres, acquis après la chute de la météorite.
Cependant certaines découvertes majeures allaient montrer que tous les constituants organiques n'étaient pas des contaminants. D'abord les travaux de Miller et Urey en 1953 ont montré que la synthèse abiotique des acides aminés dans certaines conditions favorables était possible. Ensuite la chute de Murchison en Australie en 1969 a permis de nouvelles découvertes. Murchison a été collectée au moment où le programme lunaire de la NASA avait permis de développer des protocoles d'échantillonnage et de collection des échantillons extraterrestres très propres pour réduire au maximum la contamination terrestre. Très vite, il a été montré que cette météorite contient des acides aminés, certains communs sur Terre, d'autres étant inconnus dans l'environnement naturel terrestre. Les arguments structuraux (mélange racémique) et isotopiques (enrichissement en D et 15N par rapport aux composés terrestres) confirment qu'ils sont bien extraterrestres. Au cours des années qui ont suivi, de nombreuses équipes ont décrit le contenu organique des chondrites carbonées, constitué d'une fraction soluble et d'une fraction insoluble.
Si les premiers auteurs ont émis l'hypothèse que cette matière organique était le résultat d'une activité biologique extraterrestre, il est communément admis aujourd'hui que cette matière organique est d'origine abiotique, c'est-à-dire produite par des processus purement chimiques. Par contre la question qui se pose actuellement est de comprendre si les composés organiques que l'on retrouve dans les météorites, mais aussi dans les comètes ou dans le milieu interstellaire, ont pu influencer l'apparition et le développement de la vie sur Terre, et donc pourquoi pas sur d'autres planètes. Ce problème rejoint le concept de la « soupe prébiotique » dans les océans de la Terre primitive, qui permit la formation des premières formes de vie.
Rappel sur les chondrites carbonées
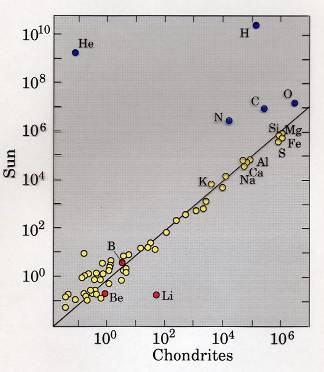
Les chondrites carbonées sont considérées comme les météorites les plus primitives du système solaire. Parmi les arguments que l'on peut citer, leur composition élémentaire est très proche de celle du soleil, qui représente la majeure partie de la matière qui a constitué le système solaire (figure 1). Cette observation montre qu'elles n'ont pas subi de profondes modifications géochimiques depuis leur formation, en particulier elles sont issues de corps parents non différenciés et très probablement petits (moins de 20 km de diamètres).
Figure 1. Comparaison entre la composition élémentaire des chondrites carbonées et celle du Soleil
Une excellente corrélation apparaît, sauf pour les éléments volatils (hydrogène, hélium, gaz rares, carbone …) qui sont difficiles à piéger dans les silicates.
Les chondrites carbonées sont caractérisées par leur richesse en carbone, en eau et en volatiles (en particulier gaz rares) par rapport aux autres chondrites. Leur minéralogie est très variable selon la classe (figure 2). Les plus hydratées, les CI (nommées ainsi à partir de la météorite modèle d'Ivuna), ne présentent pas de chondres, sont constituées de silicates hydratés, de magnétite et de troïlite (sulfure de fer). Les CM (ressemblant à Mighei) contiennent des chondres constitués de pyroxènes et d'olivine dans une matrice proche de celle des CI. Les CV (même classe que Vigarano) présentent des inclusions blanches, appelées inclusions réfractaires, assemblages de plagioclases, spinelle, pérovskite et métaux.
Comme leur nom l'indique, les chondrites carbonées sont riches en carbone (jusqu'à 5 % en masse). Ce carbone se trouve sous différentes formes : carbonates, grains de carbure de silicium, diamants, grains de graphite et matière organique. Celle-ci représente la plus grande partie du carbone. Cette matière organique est présente sous une fraction soluble dans les solvants usuels et une fraction insoluble, qui représente de 75 à 95 % de la masse totale de matière organique.
Les composés solubles
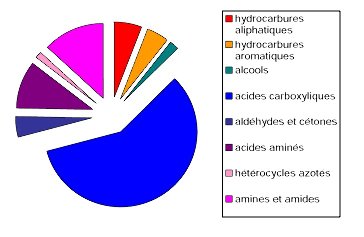
Les composés solubles dans l'eau et les solvants organiques des météorites ont surtout été décrits pour Murchison (CM2), en raison de problèmes de contamination et de plus faible abondance dans les autres chondrites carbonées. On peut extraire une multitude de composés solubles d'origine extraterrestre. Ont ainsi été mis en évidence plusieurs familles d'acides carboxyliques, des hydrocarbures linéaires et aromatiques, des alcools, des cétones et des composés azotés comme des amines, des acides aminés ou des hétérocycles azotés (figure 3).
Figure 3. Répartition des composés solubles dans la météorite de Murchison
Les composés solubles les plus abondants sont les acides carboxyliques. On distingue aussi des hydrocarbures (alcanes, composés aromatiques), des alcools, des cétones, des aldéhydes et des composés azotés comme les acides aminés. Certaines molécules sont dites d'intérêt biologique car intervenant (ou pouvant intervenir) dans les cycles biologiques connus sur Terre.
Les acides aminés
Parmi les composés solubles, certains ont suscité plus d'intérêt que d'autres. C'est le cas des acides aminés (voir figure 4). Ils sont facilement extraits dans l'eau chaude. Dès les années 70, il a été établi que ces acides aminés n'étaient pas des contaminants, sur la base de plusieurs arguments (mélanges racémiques, composition isotopique en 13C, inconnus à l'état naturel sur Terre). Ces arguments ont permis de mettre en évidence que des acides aminés abiotiques étaient contenus dans les chondrites carbonées, associés à une part de contamination facilement mise en évidence par sa composition isotopique.
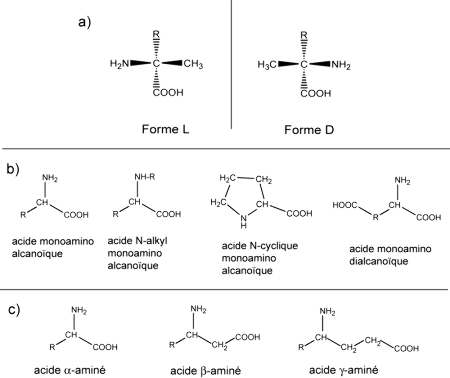
Figure 4. Les acides aminés dans les météorites
a) les formes L et D - b) les différents types d'acides aminés extraterrestres (ne sont représentés que des acides α-aminés) - c) acides α-, β- et γ- aminés (R représente une chaîne alkyle).
Depuis, 74 acides aminés ont été mis en évidence dans Murchison pour une teneur estimée à 60 ppm. Sur ce nombre, 8 sont constitutifs des protéines (alanine, glycine, valine, leucine, isoleucine, proline, acide aspartique et acide glutamique), 11 sont moins communs (par exemple la β-alanine ou l'acide γ-aminobutyrique) et les 55 autres n'existent pas dans le monde vivant sur Terre. Leurs caractéristiques moléculaires les distinguent des acides aminés terrestres. D'abord, le nombre de carbones dans ces composés va de 2 à 8, on remarque que l'abondance du composé décroît quand le nombre de carbones augmente. De plus les formes ramifiées sont prédominantes. Une grande diversité structurale est observée, avec pratiquement tous les isomères possibles détectés, même si les acides α-aminés sont plus abondants que les formes β ou γ (position du groupe NH2 par rapport au groupe COOH). Il est important de noter que les acides aminés ne sont détectés que dans les chondrites carbonées à matrice argileuse.
Contrairement aux acides aminés terrestres, où seulement la forme L des acides α-aminés existe, les acides aminés extraterrestres ont été au début détectés en mélanges racémiques, c'est-à-dire que les formes L et D sont détectées en quantités équivalentes, ce qui a ainsi donné un critère pour les attribuer à une synthèse abiotique (comme la synthèse de Strecker pour certains) et les séparer des contaminants. Il a été détecté une légère prédominance de la forme L pour l'alanine, l'acide glutamique, la proline, la leucine et l'acide aspartique. Les analyses de δ13C et δ15N ont montré que ces excès n'étaient pas un effet de contamination terrestre. Une autre étude a mis en évidence que certains acides α-méthyl α-aminés (par exemple l'isovaline) montraient eux aussi un excès de la forme L. Les réactions abiotiques de synthèse des acides aminés connues sont incapables d'être responsables de la prédominance d'une forme par rapport à l'autre. L'hypothèse la plus acceptée est liée à une irradiation des acides aminés par des rayonnements polarisés qui favoriserait une forme plutôt que l'autre. Cette observation a aussi des conséquences sur les hypothèses d'apparition de la vie à partir des molécules extraterrestres (panspermie) ; l'excès de formes L pour certains acides aminés a pu avoir une conséquence pour l'apparition de la vie en la forçant à adapter des formes L, ce qui serait à l'origine de la prédominance des formes L dans les acides aminés et les protéines des êtres vivants.
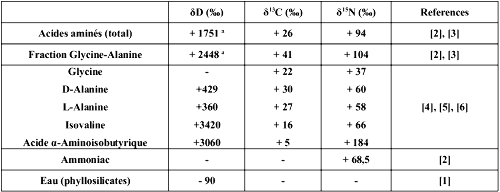
Les acides aminés montrent une composition isotopique très enrichie en isotopes lourds. Des valeurs très élevées de δD, de δ13C et de δ15N ont été mesurées (tableau ci-dessous) pour l'ensemble des acides aminés de Murchison. Ces valeurs sont interprétées comme la signature d'une origine interstellaire pour les acides aminés ou leurs précurseurs. Les données isotopiques ont été précisées plus récemment par des mesures moléculaires, par l'utilisation de la GC-irMS (chromatographie en phase gazeuse couplée à la spectrométrie de masse isotopique). Ainsi on connaît maintenant la composition isotopique de certains acides aminés individuels. Les données sur l'azote montrent que les acides aminés ont un δ15N de 60‰ en moyenne, aussi bien pour les formes L que les formes D. Cependant la glycine est appauvrie (37‰) alors que la sarcosine et l'acide α-amino-isobutyrique sont enrichis en 15N ; ces écarts sont attribués à des processus de synthèses ou des précurseurs différents des autres acides aminés ou à des fractionnements isotopiques différents. Les valeurs de δ13C des composés individuels montrent que le δ13C diminue quand le nombre de carbones augmente, pour les acides α-aminés. Ces données suggèrent une synthèse des acides aminés ou de leur précurseur par addition de carbones contrôlée cinétiquement, les composés contenant du 12C réagissant plus rapidement que ceux contenant du 13C. Il a ensuite été mis en évidence que les acides α-, β- et γ- aminés ne montrent pas la même tendance, ce qui peut être interprété comme la signature d'un processus de synthèse différent. Enfin les mesures moléculaires de δD ne montrent pas de tendance flagrante et ne sont pas encore interprétées en terme de processus de synthèse. Elles montrent cependant une très forte variabilité d'un acide aminé à l'autre, les acides aminés substitués étant plus riches en D que les chaînes linéaires.
Les autres composés « d'intérêt biologique »
En plus des acides aminés, d'autres composés pouvant avoir une relation avec le monde biologique ont été détectés. Ainsi, récemment, une série de sucres et de molécules dérivées (polyols avec fonctions acide ou alcool à la place de la fonction cétone ou aldéhyde) a été reportée. L'abondance est similaire à celle des acides aminés, tout comme eux une diversité d'isomères et un enrichissement en isotopes lourds sont observés. Il est important de noter qu'aucun de ces sucres n'existe dans le monde vivant sur Terre.
Parmi les composés azotés, des purines, des pyrimidines, des quinolines et des pyridines sont détectées. Ces composés peuvent intervenir dans la formation de molécules de type bases azotées, et ont donc pu participer à la synthèse dans des environnement prébiotiques à la formation de molécules de type ARN ou ADN.
Il existe donc dans les météorites une multitude de composés qui ont pu participer à l'apparition de la vie sur Terre et dans d'autres environnements du système solaire. Il faut souligner que la plupart de ces composés, bien que très proches, ne sont pas présents dans le monde vivant connu sur Terre. Ceci signifie que s'ils ont effectivement permis l'apparition de la vie, son évolution a permis l'apparition d'autres composés différents de ces "précurseurs".
Les autres composés solubles extraterrestres
On ne trouve pas que des molécules dites « d'intérêt biologique » dans les météorites. Les composés les plus abondants sont des acides carboxyliques. On trouve aussi des hydrocarbures comme des alcanes, ou des composés aromatiques polycycliques. Une famille d'alcools est aussi présente.
Tous les composés solubles ont cependant des propriétés similaires :
- une diversité structurale, tous les isomères possibles sont détectés, sans prédominance d'une forme ou d'une autre ;
- une abondance qui décroît quand la taille de la molécule augmente ;
- un enrichissement en isotopes lourds : D, 13C et 15N.
Ces critères permettent donc sans ambiguïté de distinguer les composés solubles extraterrestres des contaminants terrestres.
La matière organique insoluble (MOI)
La matière organique dans les chondrites carbonées est majoritairement présente sous la forme d'une macromolécule insoluble dans les solvants usuels (eau et solvants organiques). Elle représente en effet 75 à 95% en masse de la matière organique totale des chondrites carbonées. Elle est isolée après extractions aux solvants (pour éliminer la fraction soluble) et attaque acide (HF/HCl) des météorites qui vise à détruire la matrice minérale. Le résidu obtenu par ce traitement est très enrichi en matière organique insoluble mais peut parfois contenir jusqu'à 50% de minéraux réfractaires (oxydes par exemple) ou protégés par la matière organique. Cette MOI est considérée comme le réservoir majeur de gaz rares dans les chondrites carbonées, elle contient aussi des grains dit "présolaires", c'est-à-dire plus vieux que le système solaire, sous la forme de grains de carbures de silicium, de nanodiamants ou de grains de graphite.
Les techniques classiques de géochimie organique utilisées pour caractériser les kérogènes ou les charbons terrestres ont été appliquées à la MOI. À cause de ses propriétés physico-chimiques, elle est moins bien connue que la fraction soluble. Deux approches sont classiquement utilisées pour l'étudier : une approche spectroscopique, qui donne accès à une vue globale et moyennée de la MOI sans la dégrader, et une approche par dégradations (soit thermiques soit chimiques) qui offre l'avantage d'apporter des informations moléculaires plus précises mais seulement sur la partie la moins réfractaire à ces traitements. Ces informations moléculaires sont complétées par des données isotopiques en particulier du carbone et de l'hydrogène. Des observations microscopiques (photonique et électronique) ont aussi été effectuées.
L'étude moléculaire
Les analyses élémentaires effectuées sur la MOI de différentes chondrites carbonées montrent qu'elle est constituée d'un squelette carboné, avec de l'hydrogène, de l'oxygène, de l'azote et du soufre (formules structurales types : C100H72O18N3,5S2 pour Orgueil et C100H70O22N3S6,5 pour Murchison). La MOI a été analysée par oxydations chimiques et pyrolyses couplées à la chromatographie en phase gazeuse. L'identification des fragments est rendue possible par l'utilisation de la spectrométrie de masse moléculaire. La détermination des fragments issus de la dégradation d'une macromolécule insoluble permet de reconstituer sa structure, plus précisément de déduire ses unités structurales. En effet ces attaques thermiques ou chimiques n'ont pas les rendements suffisants pour « solubiliser » toute la MOI. On analyse seulement la fraction la plus labile de la MOI. Ces analyses doivent ensuite être complétées par des études spectroscopiques comme par exemple par RMN à l'état solide ou par spectrométrie infra-rouge.
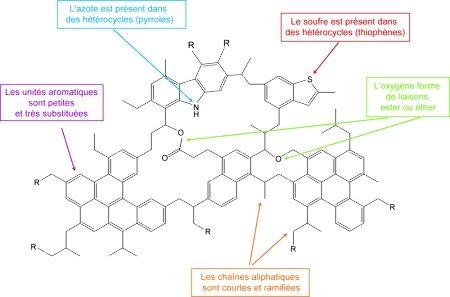
Les données récoltées au cours des 25 dernières années permettent de dresser un modèle moléculaire de la MOI des CI et CM. Il apparaît que sa structure moléculaire (voir figure 5) est constituée d'unités aromatiques comportant au maximum 10 cycles aromatiques (noyaux benzéniques) reliées entre elles par des chaînes aliphatiques courtes (jusqu'à 6 carbones) et ramifiées (avec des groupements méthyles ou éthyles, avec parfois des ramifications). La structure est donc très réticulée, c'est-à-dire que de nombreuses interconnexions sont présentes entre les différentes unités aromatiques. L'oxygène semble faire partie des liaisons entre les unités aromatiques sous la forme de fonctions éther ou ester. L'azote et le soufre semblent être inclus dans les unités aromatiques sous la forme d'hétérocycles azotés (noyaux pyrroles) et soufrés (noyaux thiophènes). Ainsi, contrairement à ce qui avait été proposé avec l'étude des premiers échantillons extraterrestres, bien qu'ayant une composition élémentaire similaire aux kérogènes et charbons terrestres, la MOI des chondrites carbonées a une structure très différente, héritée d'un processus très différent de celui qui a donné les MO fossiles terrestres.
Figure 5. Principales caractéristiques moléculaires de la MOI résumées dans un schéma "qualitatif
R représente un groupe aromatique ou aliphatique.
Une caractéristique structurale supplémentaire distingue la MOI des kérogènes et charbons terrestres. Les fragments obtenus par dégradation thermique ou chimique de la MOI possèdent des propriétés communes avec les composés solubles extraterrestres : plus leur nombre de carbone augmente, plus leur abondance diminue et tous les isomères possibles sont détectés sans prédominance d'une forme ou d'une autre. Ceci prouve que la MOI a été synthétisée par un processus abiotique, contrairement aux kérogènes et aux charbons terrestres qui proviennent de la maturation de matière organique fossile d'origine végétale, qui a gardé les traces de la spécificité isomérique des processus biologiques.
L'utilisation de la RPE (Résonance Paramagnétique Electronique) a permis de mettre en évidence la présence de radicaux (avec un électron célibataire) et de diradicaloïdes (deux électrons célibataires) organiques dans la MOI. La signature en RPE de la MOI est très différente des échantillons organiques terrestres, de plus elle contient des régions très enrichies en radicaux alors que dans la matière organique des sédiments terrestres les radicaux sont répartis de manière homogène.
La MOI des autres classes de chondrites carbonées est beaucoup moins bien connue car elle semble être beaucoup plus aromatique et donc plus résistante aux techniques d'étude. De plus la teneur en matière organique et l'abondance de ces météorites est trop faible pour permettre leur étude avec les outils actuels de géochimie organique.
Les études structurales
Ces études moléculaires ont été confortées par des observations en microscopie électronique. L'observation en microscopie électronique à transmission à haute résolution (METHR) permet d'observer le profil des feuillets aromatiques dans la MOI. Une méthode d'analyse d'image permet d'accéder à des données structurales quantitatives (longueur des feuillets, nombre de feuillets empilés, distances interfeuillets, …). Ces données ont confirmé la taille moyenne proposée à partir des études par RMN 13C à l'état solide. En METHR, la MOI d'Orgueil et de Murchison apparaît comme une structure homogène peu organisée, avec des plans aromatiques assez écartés et formant des empilements d'unités aromatiques limités à 2 à 4 feuillets. Par contre, dans les CV (par exemple Allende) ou les CO, la MOI est plus hétérogène : une partie montre des structures similaires à celles des CI et CM mais on visualise aussi des carbones mieux organisés formés d'empilements d'un nombre plus important de feuillets plus longs et plus plans, la distance inter-feuillets tendant à se rapprocher de celle du graphite (0.335 nm) comme le montrent des plis de lamelles de graphite (figure 6). Cette évolution est interprétée comme étant la conséquence de l'effet d'un métamorphisme thermique qui aurait affecté les corps parents des chondrites de types 3 à 6.
Figure 6. Images en microscopie électronique à transmission haute résolution de la MOI de Kainsaz (CO3)
Chaque image représente un carré de 50 nm de côté. Sur ces images apparaissent des franges représentant le profil des feuillets polyaromatiques. -A) carbone microporeux ; les parois des micropores sont formées de l'empilement de quelques feuillets. -B) carbone microporeux un peu plus organisé, avec domaines d'empilement plus grands : le nombre de feuillets empilés et la longueur des feuillets sont un peu plus grands que dans A. -C) carbone très graphitisé : les feuillets sont longs et plans, les empilements sont formés de plusieurs dizaines de feuillets et la distance interplans est minimale et proche de celle du graphite (0,335 nm).
L'utilisation de la spectrométrie Raman confirme ces observations : le spectre Raman de la MOI des chondrites de type CO ou CV montre une augmentation de l'organisation structurale et une diminution des défauts quand le degré de métamorphisme augmente (contrainte thermique plus importante).
Les données isotopiques
L'analyse isotopique de la MOI a été menée dans le but de comprendre l'origine et l'évolution de la MOI. On connaît ainsi les rapports D/H, 13C/12C et 15N/14N globaux de la MOI. Très récemment, les valeurs du D/H et du 13C/12C ont été mesurées de manière spécifique, c'est-à-dire sur des fragments moléculaires de la MOI. Ce genre d'études permet de déterminer de manière précise les rapports isotopiques au niveau moléculaire. Toutes ces mesures montrent que la MOI est enrichie en isotopes lourds. Ceci est particulièrement remarquable pour le rapport D/H. Celui-ci varie de 260 à 540 .10-6 (c'est-à-dire que le δD correspondant varie de 650 à 2500‰) suivant les chondrites carbonées. Cet enrichissement important est le signe de processus de type interstellaire : réactions d'échanges se déroulant à basse température dans des environnements soumis à des rayonnements UV intenses. Les forts enrichissements en D seraient hérités de processus précédant la formation des corps parents des chondrites carbonés, car une fois que la MO est incorporée au corps parent, celui-ci la protège des rayons UV. Le débat actuel porte sur la localisation de ces réactions d'enrichissement : dans un environnement interstellaire, ce qui impliquerait que la MOI soit un « polluant » organique de la nébuleuse qui a formé le système solaire, donc qu'elle soit formée avant la nébuleuse, ou bien elles ont eu lieu dans les premiers instants du système solaire, en périphérie de la nébuleuse où le gaz est froid et les rayonnements UV importants. Dans ce dernier cas, la synthèse de la MOI serait contemporaine de celle des premiers solides « solaires ». Récemment l'utilisation des sondes ioniques à l'échelle nanométriques (NanoSIMS) a permis de mettre en évidence des zones extrêmement enrichies en D dans la MOI avec un rapport D/H allant jusqu'à 1200.10-6 (figure 7). Leur signification est débattue.
Figure 7. Image NanoSIMS en rapport isotopique D/H
Cette image représente une région de 40 sur 40 μm. Cette image montre la présence de régions très riches en D, mais aussi très petites. Ces régions sont nommées hot spots et apparaissent en couleur très claire.
Les mesures individuelles de δ13C sur les fragments de la MOI montrent un lien génétique probable entre cette dernière et les hydrocarbures aromatiques solubles contenus dans les météorites. Ces hydrocarbures pourraient avoir été formés par dégradation d'une partie labile de la MOI.
L'origine de la MOI ?
De nombreux critères moléculaires et isotopiques rapprochent la MOI de la matière organique détectée dans les milieux interstellaires. Tout d'abord son caractère aromatique très marqué. Parmi les espèces organiques détectées dans l'espace, on trouve des HAPs (Hydrocarbures Polyaromatiques). Le parallèle avec la MOI a été rapidement fait même si les HAPs interstellaires sont majoritairement plus gros (plus de cycles) que les unités polyaromatiques de la MOI. Il faut toutefois noter que les plus petits PAHs sont connus pour être détruits par un fort rayonnement UV ; les unités aromatiques des météorites pourraient donc représenter la distribution initiale. Une autre propriété de la matière organique dans les milieux interstellaires est son enrichissement en deutérium. Ceci a conduit de nombreux auteurs à proposer une origine interstellaire pour la MOI et certains composés solubles à cause de leur enrichissement en deutérium. Cependant les enrichissements en D observés dans les molécules organiques interstellaires sont beaucoup plus importants que ceux mesurés dans la MOI. L'origine de la MOI est donc toujours sujette à débat.
Il apparaît cependant que l'histoire de la MOI est complexe, car elle a sûrement été affectée par de nombreux événements comme la formation du système solaire et la condensation des premiers solides, l'altération hydrothermale ou le métamorphisme haute température sur le corps parent, les irradiations, etc. On est donc encore loin d'avoir un scénario accepté par tous sur l'origine de la MOI et son évolution entre sa formation et aujourd'hui.
Conclusion
Les chondrites carbonées contiennent donc une grande variété de composés organiques, très différents des composés terrestres et qui sont très probablement d'origine abiotique. Cependant de nombreux auteurs proposent que cette matière organique ait pu servir de substrat au développement de formes de vie primitives sur Terre ou ailleurs dans le système solaire. En effet on peut facilement imaginer que ce contenu organique ait pu être apporté sans être dégradé sur la Terre Primitive et ainsi participer, au travers de la « soupe prébiotique » océanique, à l'apparition des premières formes de vie terrestres. Les estimations montrent en effet que la quantité de matière organique d'origine extraterrestre apportée sur Terre depuis sa formation est supérieure à la biomasse vivante actuelle. Cet apport continu de matière organique extraterrestre se déroule encore aujourd'hui.
Quelques références
Voir aussi l'article L'origine de la vie : apports de la géologie et de l'astronomie, par Pierre Thomas.
Articles dont sont tirées les données isotopiques du tableau.
- [1] M. H. Engel , S. A. Macko, J. A. Silfer, 1990. Carbon isotope composition of individual amino acids in the Murchison meteorite. Nature 348, 47-49
- [2] M. H. Engel , S. A. Macko, 1997. Isotopic evidence for extraterrestrial non racemic amino acids in the Murchison meteorite. Nature 389, 265-267
- [3] S. Pizzarello, R. V. Krishnamurthy, S. Epstein, J. R. Cronin, 1991. Isotopic analysis of amino acids from the Murchison meteorite. Geochimica et Cosmochimica Acta 55, 905-910
- [4] S. Pizzarello, X. Feng, S. Epstein, J. R. Cronin, 1994. Isotopic analysis of nitrogenous compounds from the Murchison meteorite : ammonia, amines, amino acids and polar hydrocarbons. Geochimica et Cosmochimica Acta 58, 5579-5587
- [5] S. Pizzarello, Y. Huang, 2005. The deuterium enrichment of individual amino acids in carbonaceous meteorites : a case for the presolar distribution of biomolecule precursors. Geochimica et Cosmochimica Acta 69, 599-605
- [6] F. Robert, S. Epstein, 1982. The concentration and isotopic composition of hydrogen, carbon and nitrogen in carbonaceous meteorites. Geochimica et Cosmochimica Acta 46, 81-95
Autres articles.
- François Robert, 1997. Les espèces chimiques du carbone dans les milieux extraterrestres, in Le Carbone dans tous ses états, P. Bernier & S. Lefrant (eds), Gordon & Breach Science Publishers, 83-126.
- Michel Maurette, 2001. La matière extraterrestre primitive et les mystères de nos origines, in L'environnement de la Terre primitive, M. Gargaud, D. Despois et J.-P. Parisot (eds), Presses universitaires de Bordeaux, 99-127
- Jacques Reisse, 2001. À propos de l'origine de la matière organique sur la Terre primitive et son évolution durant la période prébiotique, in L'environnement de la Terre primitive, M. Gargaud, D. Despois et J.-P. Parisot (eds), Presses universitaires de Bordeaux, 323-342
- S. Pizzarello, G.W. Cooper, G.J. Flynn, 2006. The nature and distribution of the organic material in carbonaceous chondrites and interplanetary dust particles, in Meteorites and the Early Solar System II, D. Lauretta, H.Y. McSween (eds), University of Arizona Press, 625–651
- I. Gilmour, 2003. Organic matter in meteorites, in Treatise on geochemistry, volume 1 : Meteorites, Comets, and Planets, A.M. Davis (ed), Elsevier
- Une page web en anglais, sur le site du remote sensing tutorial du centre Goddard Space Flight Center de la NASA.
Remarque : signification du δ : c'est l'écart relatif entre le rapport isotopique d'un échantillon et celui d'une référence, il s'exprime en ‰ suivant la formule suivante :
Dans le cas du δD, la référence est le SMOW (Standard Mean Ocean Water), qui a un D/H=155,76.10-6.