Image de la semaine | 10/10/2011
Les fers rubanés (Banded Iron Formation) de l'Archéen de Barberton, groupe de Fig Tree (-3,26 à -3,22 Ga), Afrique du Sud
10/10/2011
Résumé
Fers rubanés (BIF) et oxydation de l'océan.
Les lits gris, plus ou moins brillants, à éclat plus ou moins métallique, sont constitués d'hématite (Fe203) quasiment pure. Altérées ou hydratées, ces couches d'oxydes ferriques peuvent se colorer en brun-rouge foncé. Les lits roses ou « rouge brique » sont constitués de silice, plus ou moins colorée en rose ou rouge par des traces d'hématite. Certains bancs de silice ne sont pas continus. La pièce de 20 centimes d'euros donne l'échelle. Les bancs de cet échantillon, leurs couleurs et leurs épaisseurs sont tout à fait représentatifs des fers rubanés classiques.
L'échelle est donnée par le couteau suisse. On y retrouve des lits d'hématite gris ou bruns-rouges foncés, alternant avec des lits de silice roses ou rouges (couleur très variable suivant les endroits). Tectonisées, les couches ont un fort pendage vers le Sud. | L'échelle est donnée par le couteau suisse. On y retrouve des lits d'hématite gris ou bruns-rouges foncés, alternant avec des lits de silice roses ou rouges (couleur très variable suivant les endroits). Tectonisées, les couches ont un fort pendage vers le Sud. |
L'échelle est donnée par le pied d'un géologue. On y retrouve des lits d'hématite gris ou bruns-rouges foncés, alternant avec des lits de silice roses ou rouges (couleur très variable suivant les endroits). Tectonisées, les couches ont un fort pendage vers le Sud. | L'échelle est donnée par un géologue et son pied. On y retrouve des lits d'hématite gris ou bruns-rouges foncés, alternant avec des lits de silice roses ou rouges (couleur très variable suivant les endroits). Tectonisées, les couches ont un fort pendage vers le Sud. |
L'échelle est donnée par le couteau suisse, le pied d'un géologue ou des personnages. On y retrouve des lits d'hématite gris ou bruns-rouges foncés, alternant avec des lits de silice roses ou rouges (couleur très variable suivant les endroits). Tectonisées, les couches ont un fort pendage vers le Sud. | |
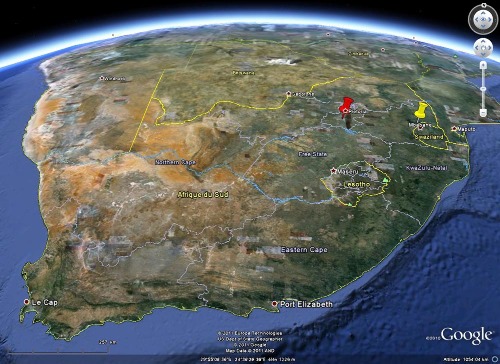
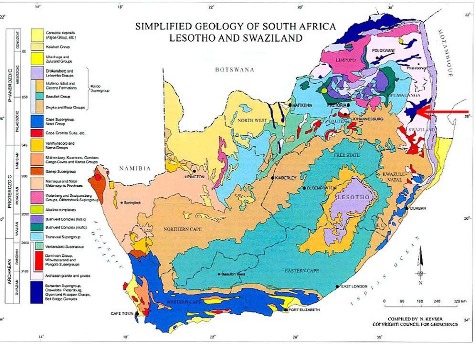
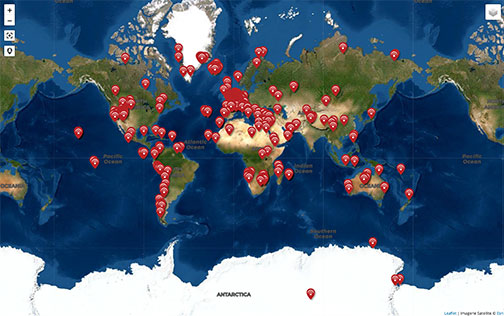
Figure 7. Localisation des fers rubanés de Barberton, au Sud de l'Afrique L'affleurement du bord de la R 40 est indiqué par la punaise jaune. L'agglomération de Prétoria-Johannesburg est figurée par une punaise rouge. | C'est au sein de ce super-groupe de Barberton (dans la ceinture verte de même nom) que se trouvent les fers rubanés de Fig Tree. On peut noter que le groupe de Fig Tree est situé dans une région voisine de celle du Witwatersrand et de ses pyrites détritiques, de part et d'autre de Johannesburg. Source : N. Keyser, dans le site de Jean François Moyen |
La grande majorité des minerais de fer du monde est constituée de ce qu'on appelle des fers rubanés (Banded Iron Formation ou BIF, en anglais). Ces BIF existent avec plusieurs faciès, mais le faciès « classique » est constitué d'alternances de lits de silice (plus ou moins ferrugineuse) et d'hématite (Fe2O3, oxyde ferrique où le fer est sous sa forme la plus oxydée Fe3+). Ce sont toujours des formations sédimentaires marines. Ces fers rubanés sont tous d'âge archéen ou protérozoïque inférieur, à l'exception de ceux liés aux épisodes Snowball Earth (épisodes Terre boule de neige) vers -0,7 Ga (voir plus bas la figure sur les BIF au cours du temps). Dans certains BIF archéens très anciens, le fer n'est pas intégralement sous forme de Fe2O3 (Fe3+ pur) mais parfois aussi sous forme de Fe3O4, mélange de Fe2O3 (Fe3+) et de FeO (Fe2+).
Ces BIF archéens ou protérozoïques inférieurs sont de deux types.
Les BIF archéens (les plus vieux sont âgés de –3,8 Ga) forment des « petits » dépôts discontinus au sein des sédiments des ceintures vertes archéennes. Ils sont souvent plus riches en silice rouge qu'en oxyde ferrique. Il portent alors le nom de « jaspilite ».
Les BIF du Protérozoïque inférieur forment de très gros gisements ; les couches sont réparties sur de vastes surfaces et constituent la majorité des gisements d'importance économique majeure. Ils datent de -2,5 à –1,9 Ga. Il n'en existe plus après cette date, à l'exception de ceux liés aux épisodes Terre boule de neige.
Les fers rubanés présentés ici sont archéens et proviennent de la série de Fig Tree, âgée de -3,26 à -3,22 Ga. Cette série appartient au super-groupe de Barberton en Afrique du Sud (-3,55 à -3,16 Ga), l'un des trois plus vieux ensembles sédimentaires peu métamorphisés connus dans le monde.
Ne se formant plus dans la nature actuelle, on ne peut pas appliquer le principe de l'actualisme à ces roches, et l'origine de ces fers rubanés est l'objet d'interrogations et de débats depuis des dizaines d'années.
La principale interrogation concerne l'origine de ces bancs d'oxyde ferrique Fe3+, que ce soit pour les gisement de l'Archéen (époque où l'atmosphère était réduite) ou du Protérozoïque inférieur (époque de la transition atmosphère réduite / atmosphère oxydée). Le fer réduit (Fe2+) est soluble dans l'eau ; le fer oxydé (Fe3+) est insoluble. Puisque du Fe3+ (insoluble) marin a précipité à l'Archéen, c'est que l'eau de mer de cette époque contenait du fer en solution, forcément sous sa forme soluble Fe2+. Cela prouve bien que la mer de cette époque était réduite, comme l'était l'atmosphère sus-jacente (cf Les galets de pyrite de l'Archéen et teneur en dioxygène de l'atmosphère). La richesse de la mer en ions Fe2+ pouvait être générale, ou localement renforcée par un volcanisme sous-marin. Dans le cas des gisements archéens, puisque de l'hématite (Fe3+) a précipité localement, mais dans de nombreuses régions du monde entre -3,8 et -2,5 Ga, c'est que l'eau de mer habituellement réduite est localement devenue oxydante, ce qui a entraîné l'oxydation des ions Fe2+ en ions Fe3+ et leur précipitation sous forme d'hématite. On peut noter que si la majorité des BIF archéens sont « pur hématite », certains, dont ceux d'Isua, âgés de –3,8 Ga, contiennent aussi de la magnétite (Fe3O4, mélange de Fe2O3 [Fe3+] et de FeO [Fe2+]).
Deux hypothèses sont « classiquement » proposées pour expliquer cette oxydation de l'eau de mer.
- Une photolyse de l'eau par les UV solaires dégageant de l'O2, rendant de ce fait la mer oxydante. Mais pourquoi une photolyse importante alors que le soleil de l'époque était moins actif que le soleil des époques plus récentes, et pourquoi cette oxydation seulement « locale », et non pas généralisée ?
- Des « oasis » de vie photosynthétique localisés, comme des tapis ou des amas de cyanobactéries. Il s'agirait d'une photosynthèse « classique », dite photosynthèse oxygénique, accompagnée de la libération d'O2 issu de la photolyse de l'eau, lorsque celle-ci fournit les électrons – oxygène qui aurait mené ensuite de l'oxydation locale de la mer.
On peut proposer une troisième hypothèse : un des types de photosynthèse très peu fréquents (mais existants) dans la nature actuelle, voire un type de photosynthèse n'existant plus actuellement (ou n'ayant pas encore été découvert par les biologistes). Citons un type de photosynthèse actuelle (rare et connu, quoique encore assez mal, des seuls spécialistes) qui pourrait expliquer cette précipitation abondante d'oxyde ferrique : la photo-ferrotrophie où le fer fournit des électrons.
La photosynthèse classique peut s'écrire de la façon suivante : 2 H2O + photons --> O2 (gaz) + 4 e- + 4 H+.
Les électrons finissent par réduire le NADP+, tandis que les protons forment un gradient transmembranaire qui, in fine, permet la synthèse d'ATP. NADPH,H+ et ATP permettent ensuite la réalisation de réactions de carboxylation et de réduction du carbone qui constituent la fabrication de matière organique proprement dite, par exemple grâce au cycle de Calvin (il existe d'autres cycles, chez les bactéries, comme, par exemple, le cycle inverse de l'acide citrique qui est un cycle de Krebs fonctionnant à l'envers). Quel que soit le détail des réactions, on transforme, au bilan, du CO2 en glucide, de formule théorique C[H2O] ; transformation que l'on résume par : CO2 + 4 H+ + 4 e- --> C[H20] + H2O.
La photo-ferrotrophie est une photosynthèse (moins énergétiquement efficace que la photosynthèse classique) qui oxyde le fer Fe2+ (FeO) en fer Fe3+ (Fe2O3) ; elle peut s'écrire de façon très simplifiée : 2 FeO + H2O + photons --> Fe2O3 + 2 H+ + 2 e-.
Ions H+ et e- seront alors utilisés par des mécanismes voisins de ceux de la photosynthèse classique pour synthétiser des glucides à partir de CO2 ; mais ce métabolisme nécessite la présence de fer Fe2+ dans le milieu et entraînera la précipitation massive d'hématite (Fe2O3).
Source - © 2011 D'après :Jean-François Moyen, modifié
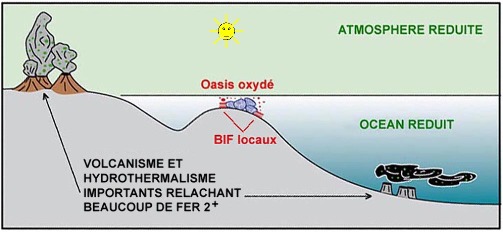
Figure 9. Schéma proposant une explication à la genèse des fers rubanés archéens
Selon cette explication, des « oasis » de vie photosynthétique créeraient des micro-environnements oxydés au sein d'une nature (atmosphère et océan) globalement réduite. Ces micro-environnements oxydés entraîneraient la précipitation locale d'oxyde ferrique (Fe2O3, avec fer Fe3+) aux dépens du fer Fe2+ présent en solution dans l'eau de mer. Cette précipitation pourrait être indirecte (photosynthèse classique libérant de l'O2, puis oxydation abiotique du Fe2+ en Fe3+) ou directe dans le cas de la photosynthèse photo-ferrotrophe.
D'autres interrogations existent, comme le devenir de la matière organique produite par cette photosynthèse et qui n'a pas pu être ré-oxydée puisque l'(éventuelle) O2 produit a été « consommé » par la précipitation de Fe2O3.
Quant aux gisements du Protérozoïque inférieur (les plus abondants) datant de -2,5 à –1,9 Ga, ils seraient dus à l'oxydation générale de l'eau de mer par l'atmosphère devenant elle-même riche en 02 à cette époque. Les modalités précises de cette oxydation généralisée, en particulier l'épaisseur de la tranche d'eau où elle a lieu est l'objet de débats scientifiques.
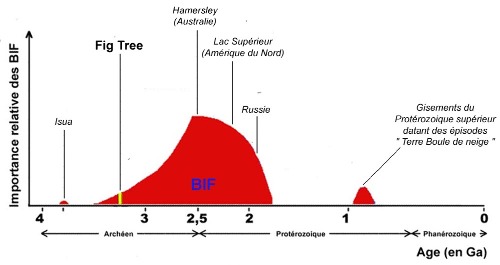
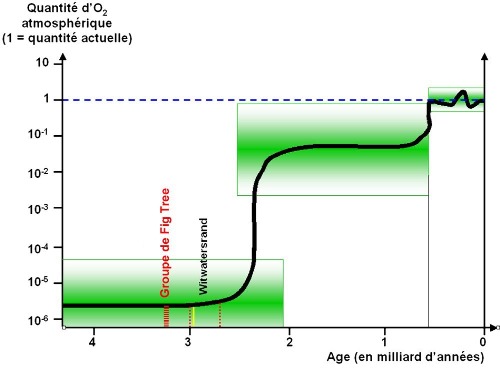
Figure 10. Évolution de l'importance relative des BIF (fers rubanés) au cours des temps géologiques Les BIF de Fig Tree sont figurés avec le trait jaune. La majorité des BIF, et les plus riche en Fe2O3, datent du Protérozoïque inférieur. D'après : C. Klein C. 1997. Igneous ferment at Hamersley, Nature 385, modifié | Figure 11. Évolution de la quantité de dioxygène dans l'atmosphère terrestre (échelle log) en fonction du temps La valeur 1 correspond à la quantité actuelle d'O2 atmosphérique, soit 21% de l'atmosphère d'aujourd'hui, c'est-à-dire 213 hPa ~106 Gt d'O2. La position du groupe de Fig Tree (-3,25 Ga) est figurée par les tiretés rouges. La position du Witwatersrand (de -2,98 à -2,71 Ga) est figurée par les deux pointillés rouges ; les conglomérats à pyrite (et or) du Witwatersrand sont figurés par le trait jaune. La précipitation d'oxydes de Fe3+ de Fig Tree a donc lieu pendant que l'atmosphère ne contenait pas d'O2. Cette précipitation a sans doute eu lieu au niveau d'un « oasis » de vie photosynthétique, photosynthèse classique ou photo-ferrotrophe. L'évolution de la teneur de l'atmosphère en O2 est l'objet de nombreuses incertitudes. La courbe présentée ici synthétise les données et les incertitudes les plus récentes (2008). Les données, comme la présence de pyrite détritique, ou de Fe2+ en solution ne permettent pas toujours de quantifier avec précision la teneur atmosphérique en O2, et de grandes incertitudes demeurent. Le trait noir et la zone vert foncé indiquent la valeur « probable » de cette teneur. Les rectangles verts indiquent le domaine d'incertitude où pourrait se trouver la valeur réelle. La « brusque » augmentation de l'O2 atmosphérique vers -2,5 Ga est selon toute probabilité une réalité. Des progrès dans les datations l'ont « légèrement vieilli » par rapport à ce qu'ont pensait il y a quelques dizaines d'années. Mais cette augmentation pourrait avoir été moins brutale que dessinée ici et s'être poursuivie jusque vers –2 Ga. Par contre, au vu des incertitudes, l'augmentation assez nette sur le schéma vers –0,7 à –0,6 Ga pourrait être largement moins brutale que ne l'indique le « trait noir », et il pourrait y avoir une augmentation relativement continue entre –2 et –0,6 Ga. L'incertitude au cours du Paléozoïque, depuis 0,6 Ga, est beaucoup plus faible ; le pic à 35% d'O2 atmosphérique à 0,3 Ga (Carbonifère) est très vraisemblablement une réalité géologique. D'après : Lee R. Kump, 2008. The rise of atmospheric oxygen, Nature 451, modifié. |
La deuxième grande incertitude concerne l'origine du rubanement hématite / silice dans le cas des BIF classiques (ou la séparation hématite / carbonates ou hématite / silicates dans le cas des autres faciès moins classiques). Là encore, deux hypothèses extrêmes sont proposées.
- Une sédimentation alternée silice-hématite, l'hématite précipitant pendant des épisodes de photosynthèse active, la silice précipitant en absence de photosynthèse. La rythmicité serait due à des rythmes d'origine astronomique, que ce soit des rythmes climatiques de type Milankowitch ou des rythmes saisonniers de type varve.
- Une séparation de type diagénétique, avec séparation en deux phases séparées d'un mélange initialement homogène silice + hématite, cette séparation étant « influencée et guidée » par des variations sédimentaires d'origine astronomique. La nature discontinue des bancs de silice sur la face de l'échantillon (figure 1) ou le remplissage d'une fissure/faille par de l'hématite sur une autre face l'échantillon (figure suivante) montrent que des migrations diagénético-hydrothermales d'hématite sont possibles.
Ces remplissages montrent la réalité d'une migration diagénético-hydrothermale de l'hématite.
Tout le super-groupe de Barberton a subi plusieurs événements tectoniques depuis son dépôt. Les plissements dans les roches litées et colorées que sont les fers rubanés donnent lieu à de superbes affleurements.
Figure 13. L'ancienne carrière de Schoongezicht, au Sud de Barberton, Afrique du Sud Cette carrière est aussi sur le bord de route R40, 4 km au Nord de l'affleurement précédent. | |
Figure 14. Vue détaillée de l'ancienne carrière de Schoongezicht, au Sud de Barberton, Afrique du Sud Cette carrière est aussi sur le bord de route R40, 4 km au Nord de l'affleurement précédent. Cette vue correspond au centre gauche de la photo générale de la carrière. On y voit de très beaux plis anisopaques. | Figure 15. Vue détaillée de l'ancienne carrière de Schoongezicht, au Sud de Barberton, Afrique du Sud Cette carrière est aussi sur le bord de route R40, 4 km au Nord de l'affleurement précédent. Cette vue correspond au centre droit de la photo générale de la carrière. On y voit la terminaison d'un très beau pli en fourreau. |
Merci à Jean François Moyen de m'avoir piloté sur ces beaux affleurements et à Marc André Selosse de m'avoir donné quelques renseignements sur les deux photosynthèses évoquées ici.
Pour finir, rappelons l'énigme de la semaine dernière.
Le Witwatersrand contient les plus importants gisements d'or du monde. Depuis sa découverte en 1886, environ 1/3 de tout l'or extrait depuis 5 000 ans par l'humanité en provient.
Un seul autre gisement de métal « usuel » dans le monde peut se « vanter » d'avoir fourni à lui seul une telle proportion de tout ce métal qu'on a extrait sur Terre depuis le début de l'âge des métaux....
Le métal en question est le mercure (Hg), le gisement est celui d'Almaden en Espagne (300 km au Sud de Madrid), en arrêt d'exploitation depuis 2008, il a produit un tiers du mercure extrait au monde. Les traces d'exploitation les plus anciennes ont été datées à -490 av. JC. (avant le début de la conquête romaine).