Article | 04/04/2000
La production biologique de méthane
04/04/2000
Résumé
Les sources biologiques du méthane, son influence sur l'environnement et l'effet de serre.
Table des matières
Les bactéries méthanogènes
En 1776, Volta montrait l'existence de « l'air combustible » des marécages : c'est le méthane contenu dans ce gaz qui est inflammable.
Figure 1. Le marais mouillé poitevin | Figure 2. Le marais mouillé poitevin |
Ce n'est que beaucoup plus tard que l'on apprit que ce gaz des marais était produit par des micro-organismes, les bactéries méthanogènes.
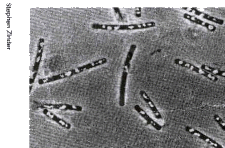
Figure 3. Exemple de bactéries méthanogènes
Ces anaérobies strictes se rencontrent dans de nombreux habitats dépourvus d'oxygène, en particulier dans les sédiments des eaux douces et des eaux marines, dans les rizières, dans les sources d'eaux chaudes d'origine volcanique (exemple de l'écosystème du Yellowstone National Park), dans le tube digestif de l'homme et des animaux mais aussi dans les stations d'épuration et les décharges. Plus de 50% du méthane issu de ces bactéries provient des ruminants et des termites des régions tropicales. Une vache en produit de 100 à 500 litres par jour, par éructation.
Minéralisations bactériennes anaérobies
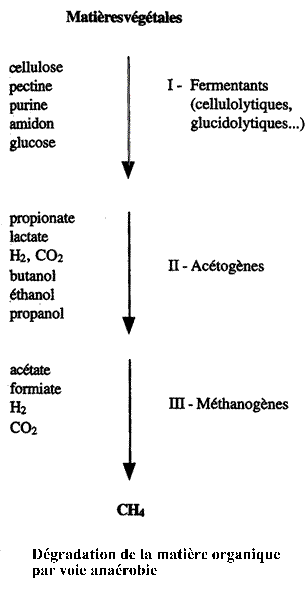
Dans l'environnement, les composés organiques sont dégradés par voie aérobie ou anaérobie en fonction de la présence ou de l'absence du dioxygène. Dans le second cas peuvent se constituer de véritables chaînes de minéralisation anaérobie au cours desquelles divers groupes de bactéries se relayent pour transformer les polymères organiques jusqu'à des molécules plus simples comme CO2, H2, H2O, CH4, etc.
On peut schématiquement distinguer trois étapes au cours de cette vie associative sans oxygène. Chaque étape est réalisée par un type de bactéries différent en l'absence d'oxygène. Fréquemment associés et complémentaires d'un point de vue métabolique, ces types bactériens forment de véritables communautés symbiotiques.
Dans un premier temps, les matières organiques complexes polysaccharidiques comme la cellulose, la pectine, la chitine, subissent une fermentation. Ces fermentations libèrent une grande variété d'acides organiques et d'alcools, mais aussi CO2 et H2.
Les métabolites organiques dérivés peuvent être convertis à leur tour dans un deuxième temps par le groupe des bactéries acétogènes. L'acide acétique est le principal produit de cette fermentation. Les bactéries acétogènes occupent un créneau intermédiaire dans les peuplements anaérobies entre les fermentants qui les précèdent et les méthanogènes, le troisième groupe d'anaérobies strictes qui leur succèdent.
Fermentation : La fermentation est une oxydation biologique au cours de laquelle l'accepteur final des hydrogènes provenant du NADH,H+ est un composé issu de la dégradation incomplète du substrat oxydable. Le substrat oxydable joue donc un double rôle : à la fois source d'énergie et accepteur final d'électrons. Dans le cas de la respiration, l'accepteur final est exogène (cas de O2 mais aussi NO3- dans la dénitrification,...). retour
Métabolismes méthanogènes
Les bactéries méthanogènes, strictement anaérobies, conduisent à la production de méthane à partir d'un mélange de gaz carbonique et d'hydrogène. Ces bactéries réduisent le CO2 (ou HCO3-) en méthane. Cette voie est génératrice d'énergie et couplée à la synthèse d'ATP. Ce métabolisme peut être considéré, de ce fait, comme un exemple d'autotrophie.
Le schéma le plus simple de production de méthane est le suivant :
CO2 + 4H2 → CH4 + 2H2O (∆G0' = - 135 kJ/mol)
L'énergie et le pouvoir réducteur proviennent d'une réaction chimique réalisée à partir de substances minérales. On parle de chimiolithotrophie.
Remarque 1 : Le passage du CO2 au CH4 s'effectue par quatre réductions successives mais peut aussi partir du méthanol ou de l'acide formique. Les électrons peuvent provenir de H2 voire, plus rarement, du fer (FeO).
Remarque 2 : La production de méthane peut également se faire à partir de la réduction d'autres molécules que le dioxyde de carbone. Les intermédiaires d'oxydation, comme le méthanol ou l'acide formique, peuvent être utilisés. Dans le cas de la méthanogenèse acétoclastique, la réduction se fait à partir de l'acide acétique :
CH3COOH → CH4 + CO2 (∆G0' = - 31 kJ/mol)
Les deux types de méthanogenèse sont liés à des bactéries du groupe des Archébactéries.
La formation de méthane est liée à des systèmes biologiques coopératifs qui procurent en continu de l'hydrogène et du gaz carbonique ou des acides organiques. Réciproquement, en retirant l'hydrogène du milieu, les méthanogènes favorisent thermodynamiquement les fermentations situées en amont dans la chaîne de dégradation.
Notez que l'une des particularités de ces voies métaboliques originales est le rôle joué par des cofacteurs qui n'existent que chez les méthanogènes. Ces cofacteurs sont sensibles à la présence de dioxygène. De simples traces de dioxygène dans le milieu tuent donc les bactéries méthanogènes.
Figure 5. Méthanogenèse par réduction du CO2
Écologie et rôle dans l'environnement
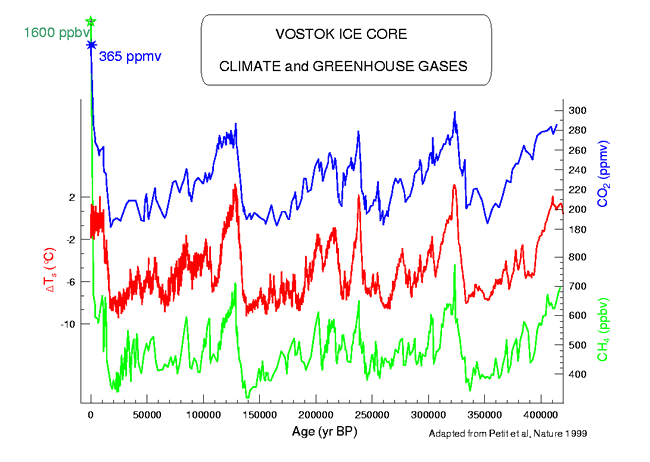
La production biologique de méthane n'est pas un épiphénomène dans la biosphère. C'est une activité majeure dans les sédiments, même profondément enfouis. Elle participe à l'équilibre biologique naturel. Le méthane contribue à l'échauffement de l'atmosphère par absorption du rayonnement infrarouge tellurique.
Tableau 1. D'après Dautray (1991)
Gaz à effet de serre | CO2 | CH4 | N2O | CFCs |
Pouvoir relatif d'absorption du rayonnement infrarouge, par unité de volume, ramené à celui du CO2 | 1 | 32 | 160 | 16.000 |
Contribution relative (en %) à l'effet de serre additif | 55 | 15 | 4 | 19 |
L'augmentation de son taux dans l'atmosphère (développement des rizières, augmentation du cheptel bovin) est un des facteurs explicatifs de l'augmentation de l'effet de serre.
Par ailleurs, des quantités importantes de méthane se trouvent au fond des océans, piégés sous forme d'hydrates de méthane. Les molécules d'eau s'arrangent autour des molécules de CH4 avec une structure cristalline très différente de la structure de la glace classique d'H2O (les conditions de pression et température ne permettant pas de faire de la glace d'H2O). On estime que leur quantité est supérieure à la somme des ressources en charbon et en pétrole de toute la planète ! Cet état n'est pas forcément stable (le méthane peut être libéré par le réchauffement de l'eau). On pense qu'au cours de l¹histoire géologique, de violents dégazages ont pu avoir lieu, renforçant l'effet de serre en peu de temps : ceci se serait produit à la fin du Paléocène (il y a 55 Ma), entraînant un fort réchauffement et la disparition de certaines espèces.
Notez enfin que, sur les fonds océaniques, les suintements de méthane abritent des communautés biologiques très riches, notamment au niveau des zones de subduction ou des grands deltas sous-marins des fleuves terrestres. Des bactéries, dites méthanotrophes celles-là, peuvent tirer leur énergie de l'oxydation du méthane produit : elles sont les producteurs primaires de chaînes trophiques variées. On trouve là de nombreuses espèces animales, notamment vivant souvent en symbiose avec ces bactéries. Pour ces écosystèmes privés de lumière, le méthane est une source d'énergie indispensable !
Bibliographie
Leclerc, H. (1995), Microbiologie générale, Doin.
Madigan, M., Martinko, J., Parker, J. (1997), Biology of microorganisms, Prentice Hall International.
Guyot, G. (1999),Climatologie de l'environnement, Ed. Dunod.
Le méthane dans les océans, Pour La Science, Octobre 1999.